Тканевая инженерия – это наука о проектировании и изготовлении тканей, включая костную и другие скелетно-мышечные ткани. В основе как тканевой инженерии, так и морфогенеза, лежат три составляющие - морфогенетические сигналы, компетентные стволовые клетки и каркасные структуры. Восстановление скелетно-мышечных тканей обобщает и эмбриональное развитие, и морфогенез. Морфогенез – это развивающаяся группа наук, изучающих образование структур, общее строение организма на пути к взрослому функционированию.
Следовательно, импульсы, вовлеченные в морфогенез, необходимо использовать при инженерии костной ткани. Морфогенетические белки кости несут широконаправленную (плеотропную) функцию в первичном формировании структур, дифференцировке клеток и восстановлении кости и суставного хряща. Способность кости к её изменениям (рекреативная способность) зависит от морфогенетических белков кости в костном матриксе. Морфогенетические белки кости действуют через рецепторы и Smads 1, 5 и 8, стимулируя клеточные линии хряща и кости. Гомеостаз тканеинженерной кости и хряща зависит от поддержания внеклеточного матрикса и биомеханики. Использование морфогенетических белков кости в генной терапии и выделение стволовых клеток в биомиметических каркасных структурах внеклеточного матрикса ведет к функциональности костной ткани. В заключение необходимо отметить, что наше время – это время увлекательных открытий в области функциональной тканевой инженерии, костных импульсов, каркасных структур и стволовых клеток.
Одна из проблем, с которыми сталкивается хирург-ортопед – восстановление и реконструкция большого сегмента кости скелета, поврежденной в результате удаления злокачественной опухоли кости или травмы. Хотя аллогенный трансплантат для крупных сегментов кости завоевал все растущее одобрение, он имеет недостатки в виде возможных трещин. Проблема трещин кости у пациентов с постклимактерическим остеопорозом, метастазами, вызванными раком молочной железы или предстательной железы, и нарушением обмена веществ, таким как при диабете, требует применения к кости принципов тканевой инженерии.
Тканевая инженерия – это наука о проектировании и изготовлении новых тканей для функционального восстановления поврежденных органов и замещения частей организма, утраченных из-за рака, различных заболеваний и травм. Среди многих тканей организма кость имеет высокую способность к восстановлению, и поэтому является эталоном для принципов тканевой инженерии в целом. В ближайшее время накопление знаний в области тканевой инженерии приведет к созданию костных имплантов с заданными параметрами для применения в ортопедической хирургии.
Тремя основными составляющими тканевой инженерии и тканевой регенерации являются сигналы, стволовые клетки и каркасные структуры. Специфичность сигналов зависит от морфогенеза тканей и индуктивных раздражителей в развивающемся эмбрионе. Они в целом воспроизводятся во время регенерации. Костные трансплантаты используются хирургами уже более ста лет. Urist сделал важнейшее открытие показав, что имплантация деминерализованных, лиофильно высушенных сегментов аллогенной кости кролика вызывала формирование новой кости. Показано, что стимулирование костеобразования является последовательным, поэтапным действием, где три ключевых этапа – хемотаксис, митоз и дифференциация имеют место. Хемотаксис – это направленное перемещение клеток под влиянием химических сигналов, высвобождаемых из деминерализованного костного матрикса. Передвижение и последующая адгезия костно-образующих клеток на коллагеновом матриксе определяется наличием в нем фибронектина.
Пик распространения клеток под действием стимуляторов роста, высвобожденных из нерастворимого деминерализованного матрикса, наблюдается на третий день. Формирование хряща достигает своего максимума на 7-8 день, за ним следует инвазия сосудов и, начиная с 9 дня, наблюдается остеогенез. Формирование кости достигает максимума на 10-12 день, на что указывает активность щелочная фосфатазы. Затем следует увеличение объема остеокальцина, костной γ-карбоксиглутаминовой кислоты, содержащей белок (BGP). Новообразованная незрелая кость заполняется красным костным мозгом к 21 дню. Деминерализованная кость за счет выделения костных морфогенетических белков, определяющих первоначальные импульсы к морфогенезу костной ткани, а также формированию множества органов помимо кости, таких как мозг, сердце, почки, легкие, кожа и зубы. Следовательно, можно относиться к морфогенетическим белками кости как к морфогенетическим белкам организма.
J.P. Fisher and A.H. Reddi, Functional Tissue Engineering of Bone: Signals and Scaffolds
Перевод Борисовой Марины
Тканевая инженерия когда-то классифицировалась как подраздел биологических материалов, но, увеличившись по своим масштабам и важности ее можно рассматривать как раздел в своем собственном праве. Ткани требуют определенных механических и структурных свойств для правильного функционирования. Термин «тканевая инженерия» также относится к коррекции выполнения конкретных биохимических функций с использованием клеток в искусственно созданной системе поддержки (например, искусственная поджелудочная железа, или искусственная печень). Термин «регенеративная медицина» часто используется как синоним тканевой инженерии, хотя в регенеративной медицине уделяется больше внимания использованию стволовых клеток для производства тканей.
Обычно тканевая инженерия, как заявил Лангер и Ваканти, рассматривается как «междисциплинарная область, в которой применяются принципы инженерии и биологии для разработки биологических заменителей, что есть восстановление, сохранение или улучшение функции тканей или целого органа». Тканевая инженерия также была определена как «понимание принципов роста тканей, и их применение для производства функциональных заменителей тканей для клинического использования». В более подробном описании говорится, что «основное предположение о тканевой инженерии является то, что использование природных биологических систем позволит достичь большего успеха в разработке терапевтических методов, направленных на замену, ремонт, обслуживание, и/или расширение функции ткани».
Клетки могут быть получены из жидких тканей, такие как кровь, множеством способов, как правило, это центрифугирование. Из твердых тканей клетки добывать труднее. Обычно ткань превращают в фарш, а затем переваривают с ферментами трипсина или коллагеназа для удаления внеклеточного матрикса, который содержит клетки. После этого клетки пускают в свободное плавание, и извлекают их как из жидких тканей. Скорость реакции с трипсином очень сильно зависит от температуры, а большие температуры наносят большой ущерб клеткам. Для коллагеназа нужны небольшие температуры, и, следовательно, здесь меньше потерь клеток, но реакция при этом занимает больше времени, а сам коллагеназ является дорогим реагентом. Клетки часто имплантируют в искусственные структуры, способные поддержать образование трехмерной ткани. Эти структуры называют строительными лесами.
Для достижения цели реконструкции ткани, строительные леса должны отвечать некоторым специфическим требованиям. Высокой пористостью и определенным размером пор, которые необходимы для содействия посева клеток и диффузии по всей структуре, как клеток, так и питательных веществ. Способность к биологическому разложению является часто существенным фактором, так как леса поглощаются окружающими тканями без необходимости хирургического удаления. Скорость, с которой происходит разложение, должна как можно больше совпадать со скоростью формирования тканей: это означает, что в то время, как изготовленные клетки создадут свою собственную природную матричную структуру вокруг себя, они уже в состоянии обеспечить структурную целостность в теле, и в конечном итоге строительные леса будут сломаны, оставив вновь образованную ткань, которая возьмет на себя механическую нагрузку.
Было исследовано множество материалов для строительных лесов (натуральных и синтетических, биоразлагаемых и постоянных). Большинство из этих материалов были известны в области медицины еще до появления в тканевой инженерии в качестве темы исследования, и уже использовались, например, в хирургии для наложения швов. Чтобы разработать строительные леса с идеальными свойствами (биосовместимость, не иммуногенность, прозрачность, и т.д.), для них были спроектированы новые материалы.
Леса также могут быть построены из натуральных материалов: в частности, были изучены различные производные от внеклеточного матрикса и их способность поддерживать рост клеток. Белковые материалы, такие, как коллаген или фибрин, и полисахариды, такие, как хитозан или гликозаминогликан (ГАГ), подходящие с точки зрения совместимости, но некоторые вопросы все еще остаются открытыми. Функциональные группы лесов могут быть полезны в доставке малых молекул (лекарств) для конкретных тканей.
Углеродные нанотрубки
Углеродные нанотрубки - это протяжённые цилиндрические структуры диаметром от одного до нескольких десятков нанометров и длиной до нескольких сантиметров, состоящие из одной или нескольких свернутых в трубку гексагональных графитовых плоскостей и заканчивающиеся обычно полусферической головкой, которая может рассматриваться как половина молекулы фуллерена.
Как известно, фуллерен (C60) был открыт группой Смолли, Крото и Кёрла в 1985 г., за что в 1996 г. эти исследователи были удостоены Нобелевской премии по химии. Что касается углеродных нанотрубок, то здесь нельзя назвать точную дату их открытия. Хотя общеизвестным является факт наблюдения структуры многостенных нанотрубок Ииджимой в 1991 г. Существуют более ранние свидетельства открытия углеродных нанотрубок. Так, например в 1974 - 1975 гг. Эндо и др. опубликовали ряд работ с описанием тонких трубок с диаметром менее 100 нм, приготовленных методом конденсации из паров, однако более детального исследования структуры не было проведено.
Группа ученых Института катализа СО АН СССР в 1977 году при изучении зауглероживания железохромовых катализаторов дегидрирования под микроскопом зарегистрировали образование "пустотелых углеродных дендритов", при этом был предложен механизм образования и описано строение стенок. В 1992 в Nature была опубликована статья, в которой утверждалось, что нанотрубки наблюдали в 1953 г. Годом ранее, в 1952, в статье советских учёных Радушкевича и Лукьяновича сообщалось об электронно-микроскопическом наблюдении волокон с диаметром порядка 100 нм, полученных при термическом разложении окиси углерода на железном катализаторе. Эти исследования также не были продолжены.
Существует множество теоретических работ по предсказанию данной аллотропной формы углерода. В работе химик Джонс (Дедалус) размышлял о свёрнутых трубах графита. В работе Л. А. Чернозатонского и другой, вышедшую в тот же год, что и работа Ииджимы, были получены и описаны углеродные нанотрубы, а М. Ю. Корнилов не только предсказал существование одностенных углеродных нанотруб в 1986 г, но и высказал предположение об их большой упругости.
Структура нанотрубок
Идеальная нанотрубка представляет собой свёрнутую в цилиндр графитовую плоскость, то есть поверхность, выложенную правильными шестиугольниками, в вершинах которых расположены атомы углерода. Результат такой операции зависит от угла ориентации графитовой плоскости относительно оси нанотрубки. Угол ориентации, в свою очередь, задаёт хиральность нанотрубки, которая определяет, в частности, её электрические характеристики.
Рис.1. Сворачивание графитовой плоскости для получения (n, m) нанотрубки
Для получения нанотрубки хиральности (n, m), графитовую плоскость надо разрезать по направлениям пунктирных линий и свернуть вдоль направления вектора R
Упорядоченная пара (n, m), указывающих координаты шестиугольника, который в результате сворачивания плоскости должен совпадать с шестиугольником, находящимся в начале координат называется хиральностью нанотрубки и обозначается. Другой способ обозначения хиральности состоит в указании угла α между направлением сворачивания нанотрубки и направлением, в котором соседние шестиугольники имеют общую сторону. Однако в этом случае для полного описания геометрии нанотрубки необходимо указать её диаметр. Индексы хиральности однослойной нанотрубки (m, n) однозначным образом определяют её диаметр D. Указанная связь имеет следующий вид:

где d 0 = 0,142 нм - расстояние между соседними атомами углерода в графитовой плоскости.
Связь между индексами хиральности (m, n) и углом α даётся соотношением:

Среди различных возможных направлений сворачивания нанотрубок выделяются те, для которых совмещение шестиугольника (n, m) с началом координат не требует искажения его структуры. Этим направлениям соответствуют, в частности, углы α = 0 (armchair конфигурация) и α = 30° (zigzag конфигурация). Указанные конфигурации отвечают хиральностям (n, 0) и (2m, m) соответственно.
Одностенные нанотрубки
Структура одностенных нанотрубок, наблюдаемых экспериментально, во многих отношениях отличается от представленной выше идеализированной картины. Прежде всего это касается вершин нанотрубки, форма которых, как следует из наблюдений, далека от идеальной полусферы. Особое место среди одностенных нанотрубок занимают так называемые armchair-нанотрубки или нанотрубки с хиральностью (10, 10). В нанотрубках такого типа две из С–С связей, входящих в состав каждого шестичленного кольца, ориентированы параллельно продольной оси трубки. Нанотрубки с подобной структурой должны обладать чисто металлической структурой.
Многостенные нанотрубки
Многостенные (multi-walled) нанотрубки отличаются от одностенных значительно более широким разнообразием форм и конфигураций. Разнообразие структур проявляется как в продольном, так и в поперечном направлении. Структура типа «русской матрёшки» (russian dolls) представляет собой совокупность коаксиально вложенных друг в друга цилиндрических трубок. Другая разновидность этой структуры представляет собой совокупность вложенных друг в друга коаксиальных призм. Наконец, последняя из приведённых структур напоминает свиток (scroll). Для всех структур характерно значение расстояния между соседними графитовыми слоями, близкое к величине 0,34 нм, присущей расстоянию между соседними плоскостями кристаллического графита.
Реализация той или иной структуры многостенных нанотрубок в конкретной экспериментальной ситуации зависит от условий синтеза. Анализ имеющихся экспериментальных данных указывает, что наиболее типичной структурой многостенных нанотрубок является структура с попеременно расположенными по длине участками типа «русской матрёшки» и «папье-маше». При этом «трубки» меньшего размера последовательно вложены в трубки большего размера.
Получение углеродных нанотрубок
Развитие методов синтеза углеродных нанотрубок (УНТ) шло по пути снижения температур синтеза. После создания технологии получения фуллеренов было обнаружено, что при электродуговом испарении графитовых электродов наряду с образованием фуллеренов образуются протяженные цилиндрические структуры. Микроскопист Сумио Ииджима, используя просвечивающий электронный микроскоп (ПЭМ) первым идентифицировал эти структуры, как нанотрубки. К высокотемпературным методам получения УНТ относятся электродуговой метод. Если испарить графитовый стержень (анод) в электрической дуге, то на противоположном электроде (катоде) образуется жесткий углеродный нарост (депозит) в мягкой сердцевине которого содержатся многостенные УНТ с диаметром 15-20 нм и длиной более 1 мкм. Формирование УНТ из фуллереновой сажи при высокотемпературном тепловом воздействии на сажу впервые наблюдали Оксфордская и Швейцарская группа. Установка для электродугового синтеза металлоемка, энергозатратна, но универсальна для получения различных типов углеродных наноматериалов. При этом существенной проблемой является неравновесность процесса при горении дуги. Электродуговой метод в свое время пришел на смену метода лазерного испарения (абляции) лучем лазера. Установка для абляции представляет собой обычную печь с резистивным нагревом, дающую температуру 1200С. Чтобы получить в ней более высокие температуры, достаточно поместить в печь мишень из углерода и направить на нее лазерный луч, попеременно сканируя всю поверхность мишени.
Таким образом, группа Смолли, используя дорогостоящие установки с короткоимпульсным лазером, получила в 1995 г. нанотрубки, "значительно упростив" технологию их синтеза. Однако, выход УНТ оставался низким. Введение в графит небольших добавок никеля и кобальта позволило увеличить выход УНТ до 70-90%. С этого момента начался новый этап в представлении о механизме образования нанотрубок. Стало очевидным, что металл является катализатором роста. Так появились первые работы по получению нанотрубок низкотемпературным методом - методом каталитического пиролиза углеводородов (CVD), где в качестве катализатора использовались частицы металла группы железа. Один из варианов установки по получению нанотрубок и нановолокон CVD методом представляет собой реактор, в который подается инертный газ-носитель, уносящий катализатор и углеводород в зону высоких температур. Упрощенно механизм роста УНТ заключается в следующем. Углерод, образующийся при термическом разложении углеводорода, растворяется в наночастице металла.
При достижении высокой концентрации углерода в частице на одной из граней частицы-катализатора происходит энергетически выгодное "выделение" избыточного углерода в виде искаженной полуфулереновой шапочки. Так зарождается нанотрубка. Разложившийся углерод продолжает поступать в частицу катализатора, и для сброса избытка его концентрации в расплаве нужно постоянно избавляться от него. Поднимающаяся полусфера (полуфуллерен) с поверхности расплава, увлекает за собой растворенный избыточный углерод, атомы которого вне расплава образуют связь С–С представляющую собой цилиндрический каркас-нанотрубку. Температура плавления частицы в наноразмерном состоянии зависит от ее радиуса. Чем меньше радиус, тем ниже температура плавления. Поэтому, наночастицы железа, с размером порядка 10 нм находятся в расплавленном состоянии ниже 600С. На данный момент осуществлен низкотемпературный синтез УНТ методом каталитического пиролиза ацетилена в присутствии частиц Fe при 550С. Снижение температуры синтеза имеет и негативные последствия. При более низких температурах получаются УНТ с большим диаметром (около 100 нм) и сильно дефектной структурой типа "бамбук" или вложенные наноконусы. Полученные материалы только состоят из углерода, но к экстраординарным характеристикам (например, модуль Юнга) наблюдаемым у одностенных углеродных нанотрубок, получаемых методом лазерной абляции или электродуговым синтезом, они даже близко не приближаются.
В будущем, как говорят фантасты, для излечения от недуга нужно будет всего лишь зайти в аптеку, похожую на склад с запчастями. И выбрать нужную полку. Вот здесь запасные глаза, вот печень, почки, а в этом ящике руки и ноги разных размеров Не отстают от писателей и голливудские фантазеры, они тоже подливают масла в огонь этой темы: эффектно отрастающие новые руки и ноги супергероев впечатляют. Но в жизни, разумеется, все гораздо прозаичнее, нежели на экране. Хотя некоторые предпосылки к тому, чтобы в скором времени человек «примерил» биоискусственные органы, уже есть.
Тканевая инженерия активно развивающаяся отрасль медицины и биологии буквально воплощает фантастику в жизнь. Специалисты, занятые в этой области, изучая строение живых тканей, пытаются вырастить их в лабораторных условиях, чтобы затем использовать искусственно созданную ткань для трансплантации. Такое «производство» откроет очень серьезные перспективы. Стоит только вдуматься в это: заболевший (раненый, покалеченный) человек сможет быстро восстанавливаться, он получит неисчерпаемый источник для замены поврежденных органов. Ведь современные темпы урбанизации и развитие технических средств, как ни странно, подвергают жителей Земли все большим опасностям и болезням, всевозможным травмам в различных катастрофах, так что задача тканевых инженеров действительно широка вырастить кости, хрящи и органы для замены поврежденных.
Как и все разделы медицины, тканевая инженерия имеет собственную терминологию и свои методологические подходы. Любая «тканеинженерная» процедура начинается с получения исходного клеточного материала первого шага. Как правило, для этого проводят биопсию, то есть забирают у пациента, нуждающегося в биоискусственной ткани, клетки нужного типа. Однако не все клетки могут достаточно интенсивно размножаться в искусственной среде. Поэтому другой подход состоит в том, чтобы отобрать недифференцированные клетки-предшественники, так называемые стволовые клетки , которые будут созревать и специализироваться уже в лабораторных условиях. Этим определяется взаимосвязь тканевой инженерии с исследованиями стволовых клеток. Однако не следует отождествлять эти два направления биомедицинских исследований тканевые инженеры работали над своими проектами еще задолго до того, как термин «стволовые клетки» стал знаком широкой публике.
Второй шаг культивирование полученных клеток в лабораторных условиях (in vitro) с целью увеличить во много раз их количество. При этом в случае использования недифференцированных (стволовых) клеток они помещаются в специальную среду, которая индуцирует их превращение в клетки строго заданного вида. Чтобы понять, насколько это сложно, достаточно сказать, что в организме насчитывается более 200 разновидностей клеток. Для достижения нужного результата культивирование проводится в специальных биореакторах. В них не только моделируется состав газовой смеси и набор веществ в питательной среде, но и поддерживаются необходимые для развития клеток и тканей физические параметры освещенность, течение или пульсация жидкости, гравитация и т. п.
Но для выращивания живой ткани мало просто получить достаточное количество нужных клеток, необходимо, чтобы они были надлежащим образом организованы в пространстве. Поэтому следующим шагом становится формирование трехмерного каркаса носителя для искомой ткани, на котором они бы могли нормально развиваться и выполнять свои функции после пересадки в организм.
Наконец, в итоге всех этих сложных манипуляций появляется готовый биоискусственный эквивалент ткани графт, и тогда наступает последний этап его имплантация в тело пациента (графтинг). Использование собственных клеток пациента для изготовления графта основополагающий принцип тканевой инженерии. Забирая аутоклетки, врачи избегают иммунологических проблем отторжения пересаженного материала, благодаря чему шансы на удачный исход операции резко возрастают.
У истоков тканевой инженерии
Если не считать сотворения Евы из ребра Адама, то выращивание клеток и тканей началось на закате XIX века. В 1885 году немецкий эмбриолог Вильгельм Ру в течение нескольких дней смог поддерживать жизнеспособность фрагмента куриного эмбриона в искусственных условиях. Однако настоящих успехов в культивировании тканей вне организма удалось достичь только после экспериментов Р. Гаррисона в 1907 году: он предложил использовать свернувшуюся кровь или лимфу в качестве среды для развития тканей в лабораторной посуде in vitro.
В Россию этот метод пришел в 1913 году, когда сотрудник Императорской Военно-медицинской академии П.П. Авроров и его коллега А.Д. Тимофеевский смогли в течение некоторого времени выращивать клетки лейкозной крови. А годом позже этой проблемой заинтересовался великий российский гистолог Александр Александрович Максимов, профессор той же академии, который не только подтвердил данным методом унитарную теорию кроветворения, то есть доказал, что все клетки крови развиваются из общего предшественника стволовой клетки, но и заложил основу для дальнейших разработок в области культивирования тканей вне организма. На базе его результатов были выполнены сотни работ по выращиванию клеток соединительной ткани и крови, созданию тканеинженерных эквивалентов костной ткани. Его приоритет в этих исследованиях признан всемирно.
Настоящая же эра тканевой инженерии, да и собственно выделение ее как самостоятельной отрасли медицины, началась с дерзких работ К. Ваканти по совмещению в лабораторных условиях живых клеток и искусственных носителей для них, которые он предпринял в 80-х годах прошедшего столетия. На сегодня, пожалуй, не осталось ни одного человеческого органа, развитие и регенерацию которого тканевые инженеры не пытались бы «приручить».
Основа ткани
Выбор носителя для развития искусственной ткани одна из самых серьезных проблем тканевой инженерии. Его материал должен быть безопасным как для тех клеток, которые на нем будут жить, так и в целом для организма, куда потом будет пересаживаться биоискусственная ткань. В идеале материал со временем полностью замещается тканью организма. При этом он должен иметь уникальную, характерную для данного типа ткани трехмерную организацию, которая воспроизводила бы структуру межклеточного матрикса живой ткани. Например, для воссоздания полых трубчатых органов используют лишенные жизнеспособных клеток участки аналогичных органов (кишечника, трахеи, мочеточников и мочевого пузыря), полученных от крупных животных. Но в качестве таких носителей могут быть применены другие, самые разнообразные и подчас весьма неожиданные материалы.
Проще всего (если, конечно, тут вообще уместно говорить о простоте) оказалось создать биоискусственные кости. В качестве источников клеток для будущих костей используют стволовые стромальные клетки костного мозга, которые могут развиваться в клетки разных тканей, а также остеогенные (способные образовывать костную ткань) клетки иного происхождения. Настоящее поле для фантазии представляется при выборе носителя для них. В ход идут коллагены различных типов, стеклокристаллические материалы, даже кораллы. Неплохой основой служат безжизненные (трупные) кости человека и животных, а также сложные синтетические конструкции, растворяющиеся за определенный срок в организме. В последнем случае основной проблемой является синхронизация процесса остеогенеза, то есть образования костной ткани в области ее дефицита и растворения привнесенной искусственной конструкции. На сегодняшний день по всему миру выполнено уже несколько тысяч хирургических вмешательств с использованием тканеинженерных эквивалентов костной ткани.
Весьма востребована на рынке медицинских услуг клеточная и тканевая реконструкция суставного хряща. Хрящ особая ткань, которая в естественных условиях не регенерирует. По некоторым экспертным оценкам, рынок этих продуктов только в США может составлять сотни миллионов долларов в год.
Не обошли вниманием тканевые инженеры и кожу самый большой орган на теле человека. Общая площадь кожного покрова взрослого мужчины достигает 2,5 м 2 при весе 1520 кг (с учетом подкожной клетчатки). Кожа устроена достаточно сложно и выполняет ряд жизненно важных функций, вот почему при ее обширных повреждениях, помимо местных расстройств, могут наблюдаться и общие патологические проявления, подчас ставящие жизнь больного под угрозу. При сильных ожогах и длительно не заживающих язвах кожа неспособна сама восстанавливать свою целостность. На помощь приходят специалисты, у которых уже есть не только лабораторные прототипы, но и коммерческие образцы биоискусственной кожи. На сегодняшний день тысячи человек в мире уже успели воспользоваться услугами фирм, предлагающих на рынке медицинских услуг подобные тканевые препараты.Но самых фантастических результатов достигли тканевые инженеры в детской практике. Растущий организм предъявляет особые требования к созданию тканеинженерных конструкций ведь они должны расти вместе с организмом ребенка. Так, недавно немецкими учеными был создан тканеинженерный сердечный клапан. В качестве основы для клеток сосудистой стенки (эндотелия) был взят сердечный клапан взрослой свиньи. А источником клеточного материала стали клетки пуповинной крови ребенка. Между прочим, до недавнего времени пуповинную кровь при родах выбрасывали вместе с плацентой, но теперь все больше данных свидетельствует о том, что сохранение этих клеток в гемабанках в определенных случаях может дать шанс для спасения жизни человека.
Искусственная челюсть
Не так давно группа немецких специалистов из города Киль под руководством Патрика Варнке (Patrick Warnke) сообщила об успешном воссоздании нижней челюсти, которая была практически полностью удалена в связи с опухолевым поражением. Первоначально врачам пришлось создать титановый каркас челюсти, который был заполнен костным матриксом, костным мозгом пациента и факторами роста кости. Однако такой большой фрагмент не мог быть помещен сразу в область повреждения, ведь лишенные собственной сосудистой сети клетки костного мозга, в том числе и стволовые, не только бы не дифференцировались в остеобласты (клетки, продуцирующие костную ткань), но и погибли от кислородного голодания и отсутствия питательных веществ. Поэтому полученную конструкцию внедрили в мышцы спины. Это было сделано для того, чтобы в толще интенсивно снабжаемых кровью мышц сосуды сами проросли в толщу «биологического протеза». Когда это произошло, конструкцию извлекли и пересадили на должное место, предварительно соединив сосуды нижней челюсти и биопротеза микрохирургическим путем.
С каждым годом таких или подобных операций проводится все больше. Они позволяют не только восстановить функцию утраченного органа, но и обеспечить эстетический косметический эффект.
Сосуды тканям!
Одним из факторов, ограничивающих фантазию тканевых инженеров, является невозможность создания относительно больших конструкций в связи с отсутствием их адекватного кровоснабжения и иннервации (связи с центральной нервной системой). Тканеинженерные конструкции, изъятые из искусственной среды, рискуют погибнуть из-за того, что в них нет кровеносных сосудов и в теле пациента они не будут в достаточной мере снабжаться питательными веществами. Частично эту проблему можно решить методом префабрификации временного помещения созданной в лаборатории тканеинженерной конструкции под кожу или между мышц. Через некоторое время, когда сосуды прорастут весь объем графта, его выделяют с сохранением сосудов и переносят в область повреждения. Однако такой подход связан с нанесением пациенту дополнительной операционной травмы, поэтому тканевые инженеры нашли гениальное решение: биоискусственным тканям биоискусственные сосуды! Первые работы были проведены с полимерными микротрубочками, выстланными изнутри эндотелием. Такие трубочки пронизывают всю толщу созданной в лаборатории ткани. Постепенно полимер рассасывается и не мешает обмену газами и питательными веществами между кровью и клетками.
На сегодняшний день уже практически ничто не ограничивает возможностей тканевых инженеров. Созданы не только лабораторные прототипы, но и применены в клинической практике тканеинженерные эквиваленты сосков молочных желез, биоискусственный мочевой пузырь, мочеточники. Определены методические подходы к созданию легких, печени, трахеи, участков кишечника и даже кавернозных тел полового члена.
Конструирование паренхиматозных органов печени, легких и других представляет особую сложность, поскольку все клетки в них находятся в тонкой взаимосвязи и должны строго занимать надлежащее им место в трехмерном пространстве. Неожиданные положительные результаты здесь проявились при выращивании клеток во взвешенном состоянии без прикрепления к поверхности. Группа исследователей под руководством профессора Колина Макгуккина (Colin McGuckin) из Университета Ньюкасла, Великобритания, использовала вращающийся биореактор, разработанный 10 лет назад специально для Международной космической станции. Он позволяет имитировать на Земле условия невесомости и микрогравитации. Оказалось, что при культивировании в нем стволовых клеток пуповинной крови можно добиться не только их превращения в функционально активные клетки печени, но и органогенеза образования аналога печеночной ткани с присущими ей функциями.
Не менее удивительные результаты дали опыты по насыщению культуры клеток металлическими наночастицами посредством липосом, беспрепятственно проникающих через клеточную мембрану. Пребывание таких структур внутри клетки практически не оказывает на нее влияния. Зато ученые получают возможность контролировать рост клеток, воздействуя на них магнитными полями разной направленности. Таким способом удалось создать не только аналоги структур печени, но и такие сложные структуры, как элементы сетчатки глаза. Разработки тканеинженерного глаза еще находятся в самых начальных стадиях, но уже удалось получить эквиваленты отдельных его частей роговицы, склеры, радужки. Правда, проблема интеграции полученных частей пока не решена. Тем не менее в научной литературе можно встретить сведения о трансплантации светочувствительных клеток палочек и колбочек в «святая святых» глаза сетчатку, правда, пока только в экспериментальных условиях.Пожалуй, чтобы окончательно почувствовать себя всемогущими, тканевым инженерам осталось лишь научиться воссоздавать в лабораторных условиях сложные производные нервных зачатков.
В ведущих западных и отечественных лабораториях специалисты пытаются воспроизвести развитие и другого крайне трудного для восстановления органа зуба. Трудности с его созданием вызваны тем, что составляющие зуба развиваются из различных источников: часть из производных нервной системы нервного гребня, а часть из эпителиальной выстилки ротовой полости. Совместить эти источники in vitro длительное время не удавалось. На сегодняшний момент в искусственных условиях частично воспроизведены лишь ранние стадии развития зуба. Как правило, без помощи организма здесь не обойтись и после этапа лабораторной работы прообраз будущего зуба все равно приходится подсаживать в его естественное окружение альвеолу челюсти (зубную лунку) для полного «созревания» тканеинженерной конструкции.
В итоге можно сказать, что минувшее двадцатилетие ознаменовалось становлением новой отрасли биологии и медицины тканевой инженерии. Специалисты, работающие в этой области, обладают поистине уникальными качествами. Они должны быть в равной степени и врачами, и биологами, а также иметь навыки хирурга. Таковых сейчас нигде не готовят, по крайней мере, в нашей стране. Как правило, тканевые инженеры это энтузиасты, которые поставили перед собой цель претворить сказку из детства в реальность. Пока общечеловеческая проблема, которой они занимаются, далека от разрешения. Ежегодно сотни тысяч людей по всему миру погибают от хронических заболеваний, так и не дождавшись спасительной пересадки донорского органа. Сегодня, видимо, уже не найдется ученых, которые стали бы отрицать, что тканевая инженерия это медицина будущего, успехи которой имеют колоссальное значение для всего человечества. Но вместе с тем сложно найти и такого специалиста, который безоговорочно призовет всех лечиться, прибегая к методам тканевой инженерии слишком уж много вопросов и нерешенных проблем стоит перед этой очень перспективной областью знаний.
Сайты по теме
www.celltranspl.ru Сайт «Клеточные технологии в медицине». Здесь же размещается электронный журнал «Клеточная трансплантология и тканевая инженерия».
www.gemabank.ru Сайт банка стволовых клеток «Гемабанк» посвящен теме хранения и использования пуповинной крови.
organprint.missouri.edu Сайт научной группы из Университета штата Миссури, США, посвященный напечатанным на специализированном принтере искусственным органам.
В последнее время во всем мире наблюдается тревожная закономерность, которая заключающееся в росте количества заболеваний и инвалидизации людей трудоспособного возраста, что настоятельно требует освоения и внедрения в клиническую практику новых, более эффективных и доступных методов восстановительного лечения больных.
Одним из таких методов наряду с имплантацией и трансплантацией является тканевая инженерия. Клеточная и тканевая инженерия - является последним достижением в области молекулярной и клеточной биологии. Этот подход открыл широкие перспективы для создания эффективных биомедицинских технологий, с помощью которых становится возможным восстановление поврежденных тканей и органов и лечение ряда тяжелых метаболических заболеваний человека.
Цель тканевой инженерии - конструирование и выращивание вне организма человека живых, функциональных тканей или органов для последующей трансплантации пациенту с целью замены или стимуляции регенерации поврежденных органа или ткани. Иными словами, на месте дефекта должна быть восстановлена трехмерная структура ткани.
Обычные имплантаты из инертных материалов могут устранить только физические и механические недостатки поврежденных тканей, - в отличие от тканей, полученных методом инженерии, которые восстанавливают, в том числе, и биологические (метаболические) функции. То есть, происходит регенерация ткани, а не простое замещение ее синтетическим материалом.
Однако для развития и совершенствования методов реконструктивной медицины на базе тканевой инженерии необходимо освоение новых высокофункциональных материалов. Эти материалы, применяемые для создания биоимплантатов, должны придавать тканеинженерным конструкциям характеристики, присущие живым тканям. Среди этих характеристик:
- 1) способность к самовосстановлению;
- 2) способность поддерживать кровоснабжение;
- 3) способность изменять строение и свойства в ответ на факторы окружающей среды, включая механическую нагрузку.
Наиболее важным элементом успеха является наличие необходимого количества функционально активных клеток, способных дифференцироваться, поддерживать соответствующий фенотип и выполнять конкретные биологические функции. Источником клеток могут быть ткани организма и внутренние органы. Возможно использование соответствующих клеток от пациента, нуждающегося в реконструктивной терапии, или от близкого родственника (аутогенных клеток). Могут быть использованы клетки различного происхождения, в том числе первичные и стволовые клетки. Первичные клетки - это зрелые клетки определенной ткани, которые могут быть взяты непосредственно от организма-донора (ex vivo) хирургическим путем. Если первичные клетки взяты у определенного организма-донора, и впоследствии необходимо имплантировать эти клетки ему же в качестве реципиента, то вероятность отторжения имплантированной ткани исключается, поскольку присутствует максимально возможная иммунологическая совместимость первичных клеток и реципиента. Однако первичные клетки, как правило, не способны делиться - их потенциал к размножению и росту низок. При культивировании таких клеток in vitro (посредством тканевой инженерии) для некоторых типов клеток возможна дедифференцировка, то есть потеря специфических, индивидуальных свойств. Так, например, хондроциты, вводимые в культуру вне организма, часто продуцируют фиброзный, а не прозрачный хрящ.
Поскольку первичные клетки не способны делиться и могут потерять свои специфичные свойства, возникла необходимость альтернативных источников клеток для развития технологий клеточной инженерии. Таковой альтернативой стали стволовые клетки.
Стволовые клетки - недифференцированные клетки, которые имеют способность к делению, самообновлению и дифференцировке в различные типы специализированных клеток под воздействием конкретных биологических стимулов.
Стволовые клетки подразделяются на "взрослые" и "эмбриональные". Эмбриональные стволовые клетки образуются из внутренней клеточной массы развития зародыша на ранней стадии, а взрослые - из тканей взрослого организма, пуповины или даже плодных тканей. Однако существует этическая проблема, связанная с неизбежным разрушением человеческого эмбриона при получении эмбриональных стволовых клеток. Поэтому предпочтительнее "добыча" клеток из тканей взрослого организма. Так, например, в 2007 году Шинью Яманакой (Shinya Yamanaka) из Киотского университета Японии были открыты индуцированные плюрипотентные стволовые клетки (ИПСК), получаемые из покровных тканей человека (в основном, из кожи). ИПСК открывают поистине невиданные возможности для регенеративной медицины, хотя, прежде чем они всерьез войдут в медицинскую практику, предстоит решить еще немало проблем.
Для направления организации, поддержания роста и дифференцировки клеток в процессе реконструкции поврежденной ткани необходим специальный носитель клеток - матрикс, представляющий из себя трехмерную сеть, похожую на губку или пемзу. Для их создания применяют биологически инертные синтетические материалы, материалы на основе природных полимеров (хитозан, альгинат, коллаген) и биокомпозиты. Так, например, эквиваленты костной ткани получают путем направленной дифференцировки стволовых клеток костного мозга, пуповинной крови или жировой ткани в остеобласты, которые затем наносят на различные материалы, поддерживающие их деление (например, донорскую кость, коллагеновые матрицы и др.).
На сегодняшний день одна из стратегий тканевой инженерии такова:
- 1) отбор и культивирование собственных или донорских стволовых клеток;
- 2) разработка специального носителя для клеток (матрицы) на основе биосовместимых материалов;
- 3) нанесение культуры клеток на матрицу и размножение клеток в биореакторе со специальными условиями культивирования;
- 4) непосредственное внедрение тканеинженерной конструкции в область пораженного органа или предварительное размещение в области, хорошо снабжаемой кровью, для дозревания и формирования микроциркуляции внутри конструкции (префабрикация).
Матриксы через некоторое время после имплантации в организм хозяина полностью исчезают (в зависимости от скорости роста ткани), а в месте дефекта останется только новая ткань. Также возможно внедрение матрикса с уже частично сформированной новой тканью ("биокомпозит"). Безусловно, после имплантации тканеинженерная конструкция должна сохранить свои структуру и функции в течение периода времени, достаточного для восстановления нормально функционирующей ткани в месте дефекта, и интегрироваться с окружающими тканями. Но, к сожалению, идеальные матриксы, удовлетворяющие всем необходимым условиям, пока не созданы.
Перспективные тканеинженерные технологии открыли возможность лабораторного создания живых тканей и органов, но перед созданием сложных органов наука пока бессильна. Однако сравнительно недавно ученые под руководством доктора Гунтера Товара (Gunter Tovar) из Общества Фраунгофера в Германии сделали огромнейший прорыв в сфере тканевой инженерии - они разработали технологию создания кровеносных сосудов. А ведь казалось, что капиллярные структуры создать искусственно невозможно, поскольку они должны быть гибкими, эластичными, малой формы и при этом взаимодействовать с естественными тканями. Как ни странно, но на помощь пришли производственные технологии - метод быстрого прототипирования (другими словами, 3D-печать). Подразумевается, что сложная трехмерная модель (в нашем случае кровеносный сосуд) печатается на трехмерном струйном принтере с использованием специальных "чернил".
Принтер наносит материал послойно, и в определенных местах слои соединяются химически. Однако заметим, что для мельчайших капилляров трехмерные принтеры пока недостаточно точны. В связи с этим был применен метод многофотонной полимеризации, используемый в полимерной промышленности. Короткие интенсивные лазерные импульсы, обрабатывающие материал, так сильно возбуждают молекулы, что они взаимодействуют друг с другом, соединяясь в длинные цепочки. Таким образом, материал полимеризуется и становится твердым, но эластичным, как естественные материалы. Эти реакции настолько управляемы, что с их помощью можно создавать мельчайшие структуры по трехмерному "чертежу".
А для того, чтобы созданные кровеносные сосуды могли состыковаться с клетками организма, при изготовлении сосудов в них интегрируют модифицированные биологические структуры (например, гепарин) и "якорные" белки. На следующем этапе в системе созданных "трубочек" закрепляются клетки эндотелия (однослойный пласт плоских клеток, выстилающий внутреннюю поверхность кровеносных сосудов) - для того, чтобы компоненты крови не приклеивались к стенкам сосудистой системы, а свободно транспортировались по ней.
Однако прежде чем действительно можно будет имплантировать выращенные в лаборатории органы с собственными кровеносными сосудами, пройдет еще какое-то время.
Осенью 2008 года руководитель клиники Университета Барселоны (Испания) и Медицинской школы Ганновера (Германия) профессор Паоло Маккиарини (Paolo Macchiarini) провел первую успешную операцию по трансплантации биоинженерного эквивалента трахеи пациентке со стенозом главного левого бронха на протяжении 3 см.
В качестве матрикса будущего трансплантата был взят сегмент трупной трахеи длиной 7 см. Чтобы получить природную матрицу, по свойствам превосходящую все то, что можно сделать из полимерных трубок, трахею очистили от окружающей соединительной ткани, клеток донора и антигенов гистосовместимости. Очищение заключалось в 25 циклах девитализации с применением 4% -деоксихолата натрия и дезоксирибонуклеазы I (процесс занял 6 недель). После каждого цикла девитализации проводили гистологическое исследование ткани для выявления количества оставшихся ядросодержащих клеток, а также иммуногистохимическое исследование на наличие в ткани антигенов гистосовместимости HLA-ABC, HLA-DR, HLA-DP и HLA-DQ. Благодаря биореактору собственной разработки ученые на поверхность медленно вращающегося отрезка трахеи равномерно нанесли шприцем суспензию клеток. Затем трансплантат, наполовину погруженный в среду для культивирования, вращался вокруг своей оси с целью попеременного контакта клеток со средой и воздухом.
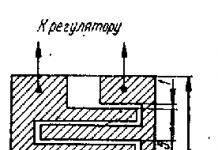
После того, как была определена пригодность разлагаемого полимера для применения в костной тканевой хирургии, он должен был быть сформирован в пористый каркасный материал. Здесь необходимы два главных этапа. Во-первых, нужно разработать способ превращения полимера в объемный материал. Во-вторых, требуется способ сделать этот материал пористым.
Изготовление материала для тканевой инженерии
Правильный способ изготовления материала, или структурирования, частично зависит от химической природы полимера. Длинные, линейные, сатурированные полимеры, такие как PLGA, обыкновенно формируются в объемный материал переплетением отдельных полимерных цепей, чтобы образовать свободносвязанную полимерную сетку. Переплетение полимерной цепи часто достигается с помощью отливки полимера в форме. Таким образом, полимер расплавляется в растворителе, потом раствор заливается в форму или оболочку, впоследствии растворитель испаряется, оставляя полимер в виде объемного материала в форме оболочки. В качестве альтернативы, вливание полимера может осуществляться с помощью нагревания, давления или и того, и другого. Так, полимер помещается в форму, нагревается до своей температуры стеклования и с применением давления принимает форму оболочки. Преимущество этих способов в том, что они относительно просты. Однако, так как материал является упругим телом только из-за переплетенных полимерных цепей, в целом материалу недостает механической прочности. Этот недостаток трудно преодолеть без изменения химического строения полимера.
Еще один способ сформировать объемный материал из линейного полимера включает образование химических связей между полимерными цепями, известное как полимерное связывание. Связывание наиболее часто производится между ненасыщенными углерод-углеродными двойными связями, следовательно, эта составляющая, или другая, дающая аналогичную реакцию, должна существовать где-нибудь в полимерной цепи. Система инициации, обычно радикальная или ионная, также необходима для обеспечения связывания. Система инициации соединяется с полимером и, в ответ на импульс, такой как тепло, свет, химический ускоритель или просто время, инициатор образует продукт, распространяющий связывание. Так как эти полимеры сформированы в объемный материал с помощью ковалентного связывания, они обычно обладают значительной механической прочностью. Более того, их способность к затвердеванию в ответ на приложенный импульс позволяет вводить эти материалы в поврежденный участок, чтобы они затвердевали на месте. Важнейший недостаток связываемых материалов в том, что растущая сложность материала в условиях множества компонентов и наличия химической реакции часто ведет к проблемам с цитотоксичностью и биосовместимостью.
Также следует заметить, что отправная точка материала может не являться полимером, а может быть меньшей молекулой, такой как олигомер или мономер. С этими меньшими молекулами материал может формироваться с помощью инициации их полимеризации. Полимеризованные мономеры могут впоследствии сформировать объемный материал посредством переплетения длинных полимерных цепей в случае с бифункциональным мономером, или разветвления сеток в случае с мультифункциональными мономерами. Преимущества и недостатки, связанные с полимеризацией мономера, такие же, как с полимерным связыванием.
Методы, описанные выше, могут применяться как к гидрофобным, так и к гидрофильным полимерам. Основное преимущество гидрофобных полимеров, таких как PLA, над гидрофильными полимерами, такими как PEG, состоит в сравнительной прочности образуемого геля. Однако, гидрофобные полимеры в целом не могут использоваться для клеточной инкапсуляции, так как гель препятствует транспортировке воды, питательных веществ и отходов к клетке и из нее. Гели, образованные из гидрофобных полимеров, обычно используются в качестве каркаса, в котором клетки и ткани присоединяются к поверхности материала более чем внутри материала. Для применения в клеточной инкапсуляции особенно полезными являются гидрофильные полимеры (39, 46-51, 59-61). Эти полимеры образуют гель, который часто содержит до 90 % воды, что допускает значительную пассивную диффузию молекул в клетку и из нее. Высокое содержание воды, к сожалению, часто влечет за собой ухудшение механических свойств геля. В костной тканевой инженерии гидрогели могут использоваться в среде, не несущей нагрузок или в качестве компонента внутри каркаса, обладающего достаточно высокими механическими качествами. Выбор между гидрофильным и гидрофобным полимерами зависит, в основном, от рассматриваемой стратегии тканевой инженерии, а также от самих тканей.
Биомиметические материалы
Последние исследования сосредоточены на биомиметических материалах. Биомиметические материалы, созданные, чтобы более точно воспроизводить структуру внеклеточного матрикса, обычно являются гидрогелями, призванными особым образом взаимодействовать с определенным видом клеток таким образом, чтобы создать искусственную ткань, обладающую необходимыми свойствами. В целом, эти материалы впервые были получены путем создания материала, практически полностью предотвращающего клеточную адгезию. Далее, сигнальные молекулы, чаще всего короткие пептидные последовательности, полученные адгезией белков и участвующие в специфичной клеточной адгезии, ковалентно связываются с материалом. В результате получается материал, допускающий прикрепляться к его поверхности или проникать в его поры только особый вид клеток.
Очень важный фактор, который часто упускается из вида, это то, что первоначальный материал должен предотвращать случайную клеточную адгезию, чтобы окончательный материал обладал специфичной адгезией. Это часто достигается путем использования гидрогеля в качестве основного материала, так как считается, что гидрофильность гидрогелей предотвращает адсорбцию гидрофобных белков, необходимую для клеточной адгезии. Дополнительные факторы, определяющие успех этой стратегии, – объединение пептидной последовательности в наполнителе, более чем на поверхности материала, ограниченное расстояние, предоставленное пептидной последовательности, таким образом, становится возможно привязать ее к рецепторам поверхности клетки, и плотность пептидных последовательностей внутри материала. Наконец, дальнейшие исследования пептидных последовательностей, специфичных для адгезии отдельных клеточных популяций, необходимы для дальнейшего успеха этой методики.
Порообразование
После того, как была разработана методика превращения полимера в твердый материал, необходимо найти способ образования пористой структуры внутри материала. Самая простая методика – включение порогена в материал перед приготовлением, а после извлечь пороген. Объем, однажды заполненный порогеном, потом остается пустым, образуя поры внутри материала. Зная плотность материала и порогена, можно вычислить пористость, контролируя вес порогена относительно материала. Этот метод, известный как выщелачивание порогена, наиболее легко выполним с использованием порогена, растворимого в воде, такого как соль, сахар или крупицы желатина, который может быть извлечен замачиванием конструкции в воде. Принцип этого метода в том, что может быть собрано достаточное количество порогена, таким образом, отдельные поры соприкасаются друг с другом, образуя связанную пористую структуру внутри материала. Связанная пористость необходима не только для своевременного извлечения порогена, но и для создания каркаса для жизнеспособных тканей. Количество порогена, необходимое для соединяемости, зависит от материала и порогена, но обычно 70 % веса конструкции занимает пороген. Наконец, порогенный метод имеет то преимущество, что связанная пористость может быть достигнута простым измерением веса каркасной конструкции до и после извлечения порогена, если вес порогена, содержащегося в каркасной конструкции, равен весу, потерянному порогенным выщелачиванием, связанность достигнута.
Вторая основная методика формирования пористой структуры включает использование газа для образования пор внутри материала. Обычно газы, такие как азот или углекислый газ, вводят в состав объемного материала во время его приготовления, продувая материал газом или образуя газ как продукт химической реакции. Другой способ – образование пузырей замороженного растворителя, которые постепенно извлекаются испарением, чтобы получить пористую структуру материала. Опять же, основной принцип этого метода – объединение достаточного объема газа для формирования связанной пористой структуры.
В настоящее время разработаны более простые технологии создания каркасных структур с определенным строением. К настоящему моменту эти методы чаще всего используются для образования пористых каркасов, таких как описанный выше, для получения каркаса случайного строения. Это случайное пористое строение имеет два недостатка. Во-первых, оно сильно ухудшает механические свойства каркаса. Это ведет к необходимости создания материалов с очень высокими механическими качествами, чтобы полученный каркас мог использоваться в костной тканевой инженерии, а это ограничивает выбор применяемых материалов. Во-вторых, не менее важно то, что случайная пористость мешает серьезным исследованиям влияния каркасной структуры на образование тканей – проблема очень серьезная для костной тканевой инженерии. Ведущие методы создания каркасов с заданным строением включают в себя техники быстрого изготовления моделей, такие как трехмерное отпечатывание и стереолитография.
J.P. Fisher and A.H. Reddi, Functional Tissue Engineering of Bone: Signals and Scaffolds
Перевод Борисовой Марины