Наиболее распространенным диагностическим методом, лежащим в основе диагностики практически всех заболеваний пищевода, желудка и двенадцатиперстной кишки является в настоящее время, эндоскопический метод – метод визуального осмотра слизистой оболочки данных органов. Большим преимуществом эндоскопии является возможность исследования тех отделов органов ЖКТ, которые трудно просматриваются рентгенологически (привратниковый канал), или патологических процессов (язвы), которые скрываются в складчатых структурах деформированной двенадцатиперстной кишки. Кроме того, облегчается диагностика поверхностных поражений слизистой оболочки с небольшими изменениями рельефа (полные и простые эрозии, небольшие полипы и т.п.).
Эндоскопическое исследование пищевода, желудка и двенадцатиперстной кишки производится с помощью фиброэндоскопов – гибких оптических приборов с волоконной оптикой (рис. 5.82). В последнее время в эндоскопию широко внедряется метод видеоэндоскопии достоинством которого является то, что весь процесс исследования выводится на экран монитора с одновременной видеозаписью.
Самым последним достижением в видеоэндоскопической технике стало применение в диагностике состояния желудочно-кишечного тракта видеоэндоскопической капсулы (рис. 5.83). Создание капсульной эндоскопии основано на самых передовых достижениях в оптике и микроэлектронике. Эндоскопическая капсула представляет собой одноразовую эндоскопическую капсулу размером 11х26 мм и весом 4 г. Капсула содержит цветную видеокамеру, 4 источника света, радиопередатчик и источник питания. Пациент перед исследованием воздерживается от приема пищи в течение 8 часов, затем принимает капсулу, запивая ее небольшим количеством воды. Принятая внутрь капсула с перистальтикой движется по ЖКТ, а вся видеоинформация записывается на закрепленный, на поясе пациента регистрирующий прибор. Далее, по окончании исследования, видеокапсула покидает организм естественным путем, а весь полученный материал обрабатывается с помощью специальной программы на компьютерной рабочей станции.
С помощью данного прибора, возможно, диагностировать весь спектр заболеваний ЖКТ, особенно тех его отделов, которые трудно доступны традиционной эндоскопии (тонкий кишечник), а также в тех случаях, когда обычная эндоскопическая процедура трудно выполнима (тяжело больные пациенты). Особенно перспективно применение эндоскопической капсулы для диагностики опухолевой патологии, во всех трех отделах тонкой кишки – двенадцатиперстной, тощей и подвздошной. Данная методика позволяет выявить скрытые источники кровотечения, раскрыть причину периодического абдоминального болевого синдрома (дивертикулярная болезнь), проследить эффективность терапевтических мероприятий.
Эндоскопический метод исследования пищевода позволяет непосредственно осмотреть слизистую оболочку органа, определить степень выраженности морфологических изменений при воспалительных, деструктивных, склеротических, стенотических, в том числе и опухолевых процессах в пищеводе.
В норме слизистая пищевода бледно-розовая, гладкая блестящая, на расстоянии 38-40 см от резцов она сменяется более яркой слизистой желудка – так называемая зубчатая или Z – линия.
При эндоскопии оценивается также состояние просвета пищевода, исключаются рубцовые сужения (белесоватые, уплотненные участки сужений), дивертикулярные расширения, язвенные, эрозивные, опухолевые процессы, их протяженность, площадь поражения, наличие осложнений – кровотечение, перфорация). При эндоскопически позитивной гастроэзофагеальной рефлюксной болезни, особенно при выраженных воспалительных изменениях (эрозии, язвы) (см. рис. 5.8) и наличии пептической стриктуры, отмечается отек, гиперемия слизистой, наложения фибрина на достаточно большом протяжении выше места сужения.
Эндоскопия является основным методом диагностики эндоскопически позитивной ГЭРБ, позволяет вовремя выявить наличие осложнений, произвести прицельную биопсию, а также контролировать результаты лечения.
Однако при эндоскопически негативной ГЭРБ, проявляющейся только клинически симптомом изжоги, обычно визуально выявить метаплазию и дисплазию слизистой оболочки пищевода (угрожающие по возникновению опухолевых процессов морфологические перестроечные процессы в эпителии пищевода) во время обычной эндоскопии бывает невозможно. Эндоскопические признаки перестройки слизистой оболочки пищевода могут отсутствовать. Для точной диагностики указанных процессов необходима дополнительная морфологическая диагностика с помощью биопсии. Биоптаты берут из 4 выбранных наугад точек по окружности пищевода, через каждые 2 см от пищеводно-желудочного перехода до зубчатой линии, а также изо всех визуально измененных участков слизистой в этой зоне.
Для более точного диагностирования характера изменений, распространенности процесса, а также для направленной биопсии в процессе эндоскопического исследования используются витальные красители (хромоэндоскопия). Для витальной окраски слизистой оболочки пищевода используются красители, которые различаются по механизму действия: абсорбирующиеся красители - раствор метиленового синего и раствор Люголя, а также контрастные красители - индигокармин.
Раствор метиленового синего активно абсорбируется клетками кишечной метаплазии, что окрашивает участки кишечной метаплазии в голубой цвет.
Раствор Люголя используется для выявления минимальных изменений слизистой оболочки пищевода. Он временно окрашивает в темно-коричневый цвет нормальный плоский эпителий. Окрашивание происходит за счет реакции с богатыми гликогеном клетками. Патологически измененные, бедные гликогеном клетки слизистой оболочки пищевода остаются неокрашенными, и протяженность его поражения становится отчетливо видна.
Раствор индигокармина не окрашивает клетки слизистой оболочки пищевода, а, распределяясь по поверхности слизистой оболочке, позволяет определить участки с измененной структурой при различных поражениях (рубцы, полипы, небольшие опухоли), в том числе позволяет визуально идентифицировать области с кишечной метаплазией и дисплазией высокой степени.
Для увеличения частоты диагностики неоплазии предложен также метод флюоресцентной эндоскопии. Существуют два варианта данного метода. Первый основан на использовании способности тканей флюоресцировать при освещении их светом определенной длины волны, что происходит благодаря эндогенным тканевым флюорофорам (здоровые ткани и неоплазия имеют различный уровень метаболизма и соответственно различные флюоресцентные спектры). Второй вариант заключается в системном или местном введение сенсибилизатора (5-аминолевулоновая кислота), накапливающегося в тканях, подвергшихся неоплазии. Флюоресцентная эндоскопия обеспечивает более точное определение очагов неоплазии для выполнения прицельной биопсии.
При злокачественных новообразованиях пищевода, экзофитно растущая опухоль, может определяться образование, растущее в просвет пищевода, перекрывающая его частично или полностью (рис. 5.84). Опухоль может иметь неровную, бугристую поверхность, участки изъязвлений, некрозов, сгустки крови. При эндофитном раке обнаруживается картина циркулярного сужения пищевода.
При ахалазии кардии, особенно в далеко зашедших случаях, обнаруживается выраженное расширение пищевода (до 10 см) с эксцентрично расположенным, сомкнутым кардиальным сфинктером и явлениями эзофагита из-за застоя содержимого.
Эндоскопический метод исследования желудка и двенадцатиперстной кишки. В норме при эндоскопическом исследовании нормальная слизистая оболочка желудка и ДПК бледно-розового или красного цвета, гладкая, блестящая с нежными (в ДПК бархатистыми) складками слизистой оболочки, расправляющимися при раздувании воздухом. В желудке во время перистальтики складки хорошо конвергируют, приобретая звездчатый характер. Слизистая луковицы имеет светло-розовый цвет, ячеистый вид и “сочный” характер. В луковице, как уже указывалось выше, складки продольные, а в остальных – циркулярные, более выраженные в дистальных отделах. Цвет слизистой оболочки в дистальных отделах с желтоватым оттенком из-за окрашивания желчью. Просвет ДПК в постбульбарных отделах имеет округлую форму, а изгибы кишки четко контурируются.
Если дуоденальный сосочек покрыт эпителием двенадцатиперстной кишки, то цвет его не отличается от окружающей слизистой ДПК, а его отверстие плохо контурируется. В случае смешанного покрытия сосочка эпителием (частично эпителий ДПК, частично – протоковый эпителий) то центральная его часть имеет ярко-розовую окраску и бахромчатый вид.
По эндоскопическим признакам воспалительные процессы в желудке и двенадцатиперстной кишке (гастрит, гастродуоденит, дуоденит) разделяются на поверхностный, выраженный, резко выраженный, а также на атрофический и эрозивный гастрит и дуоденит.
Эндоскопическими признаками воспаления являются: а) отечность; б) гиперемия; в) слизь; г) точечные геморрагии; д) контактная кровоточивость; е) феномен «манной крупы» (белесоватые зерна диаметром до 0,8 мм), а также поверхностные эрозии (единичные и множественные). Обычно степень выраженности воспаления оценивается визуально по совокупности указанных признаков и их выраженности (рис. 5.85).
О наличии атрофических процессов в слизистой оболочке желудка и двенадцатиперстной кишки, по визуальным признакам, судят по степени истончения слизистой, ее бледности, степени просвечивания сосудистой сети (см. рис. 5.25).
Предъязвенное состояние (процесс формирования язвы) характеризуется ограниченным участком гиперемии на поверхности желудка и ДПК с точечными кровоизлияниями. Затем появляются плоские (острые) эрозии, которые, сливаясь, образуют язву. Вокруг образовавшейся язвы появляется воспалительный вал (отечные, приподнятые края язвы). Язвенные дефекты чаще имеют округлую форму (рис. 5.86), реже (но чаще чем при язвенном поражении желудка) обнаруживаются линейные язвы или дефекты неправильных очертаний. Края язвы отличаются легкой ранимостью эндоскопом. Дно язвенного дефекта обычно покрыто белым или желтовато-белым налетом фибрина. Окружающая слизистая оболочка, как правило, выглядит воспаленной (отечна гиперемирована, складки ее утолщены и плохо расправляются воздухом. Слизистая может кровоточить при контакте с прибором.
При хронизации язвенного процесса или стихании явлений воспаления (II стадия развития язвенного дефекта) края язвы уплощаются, дефект приобретает неправильную форму, за счет неодновременно идущих процессов репарации, появляется конвергенция складок слизистой оболочки к краям язвы. Стихает и выраженность воспалительного процесса вокруг язвенного дефекта (уменьшаются отек и гиперемия). III стадия развития язвенного процесса – стадия рубцевания язвы. Для данной стадии характерно приобретение язвенным дефектом щелевидной формы с неглубоким дном. Вокруг язвы явления воспаления остается небольшая инфильтрация, очаговая гиперемия, единичные эрозии все еще могут сохраняться.
Фаза рубца проходит два этапа: а) фаза красного рубца; б) фаза белого рубца. Фаза «а» это участок на месте бывшей язвы ярко красного цвета с конвергенцией складок слизистой оболочки и зоной гиперемии вокруг. Форма рубца, как правило, линейная (рис. 5.87) или звездчатая. При глубоких язвах, особенно хронически-рецидивирующих, на месте красного пятна появляется рубец белесого цвета (фаза белого рубца). К этому времени конвергенция складок становится менее выраженной, уменьшается и деформация органа. В ряде случаев при полноценной эпителизации поверхности язвы трудно определить наличие места бывшей язвы, а слизистая расправляется.
Неоднократно рецидивирующие язвы оставляют, как правило, выраженную деформацию органа, неравномерное сужение ее просвета, иногда трудно пропускающее эндоскоп (для дуоденальной язвы).
Морфологическое исследование биоптатов взятых из области язвенного дефекта и удаленных от язвы регионов (слизистая ДПК и желудка с участками воспаления, метаплазии и пр.) помогает верифицировать наличие, характер и степень активности сопутствующих дуоденита и гастрита. Кроме того, позволяет забрать материал для проведения тестов на Н.pylori.
В материале, полученном с помощью биопсии со дна язвы и из ее краев, обнаруживаются бесструктурный детрит (продукт клеточного распада), скопления слизи, слущенный эпителий. Под детритными массами видны некротизированные коллагеновые волокна, затромбированные сосуды. В периульцерогенной зоне (зоне гиперемии) выявляется отек и полнокровие сосудов с мукоидным отеком и фибриноидным некрозом в их стенках, клеточная лимфоплазмоцитарная (круглоклеточная) инфильтрация стенки. Обнаруживаются также эозинофилы, нейтрофилы. Можно также обнаружить дистрофию и распад нервных элементов, атрофию желез, разрастание соединительной ткани (фиброз), а в окружающей ткани при дуоденальной язве - явления желудочной (антрального типа) метаплазии.
В стадии репарации в полости язвенного кратера обнаруживается грануляционная ткань, в стенках уменьшается, а затем исчезает круглоклеточная инфильтрация. Одновременно с краев язвы происходит «наползание» кишечного эпителия.
В сочетании с язвенным процессом в слизистой (обычно в 100% случаев), эндоскоипически определяется наличие гастродуоденита. Гастродуоденит может быть острым и хроническим, эрозивным и неэрозивным, диффузным и ограниченным (очаговым).
Очень большое значение имеет эндоскопическое исследование при диагностике язвенных кровотечений (см. рис. 5.20).
Эндоскопическое исследование помогает также диагностировать дивертикулы ДПК, которые часто локализуются в двенадцатиперстной кишке, как правило, сочетаясь с дивертикулами в других отделах ЖКТ (пищеводе, тонкой и толстой кишке). Чаще всего, до 90% случаев, дивертикулы в ДПК локализуются в нисходящей ее части, рядом с головкой поджелудочной железы, а также в области ее нижней горизонтальной части (см. рис. 5.17).
При эндоскопии желудка и ДПК можно обнаружить полипы слизистой оболочки (рис. 5.88) и другие опухолевые новообразования. Рак желудка чаще локализуется в антральном отделе желудка, на малой кривизне и, реже, в кардиальном отделе.
Экзофитный рост опухоли проявляется в виде полипозного (выступающая в просвет желудка опухоль на широком основании, ярко красного, серо-желтого и др. цвета) и изъязвленного рака (блюдцеобразная язва с подрытыми краями и дном покрытым серым налетом, нередко со сгустками крови) (рис. 5.89).
Эндофитный рак (инфильтративно-язвенный рак) также имеет вид язвенного дефекта с неровным, бугристым дном, но более плоского по форме, без выраженного окружающего язву валика.
Диффузный (инфильтративный) рак характеризуется наличием ригидных, неподвижных складок слизистой оболочки органа, бледно-серым цветом слизистой оболочки.
Эндоскопическое исследование толстой кишки. Эндоскопическое исследование толстой кишки – колоноскопия проводится специальным эндоскопом (колоноскопом) длиной 185 см. Данный прибор при адекватной подготовке больного и отсутствии препятствий для проведения процедуры (опухоли, стриктуры и пр.) позволяет осмотреть всю толстую кишку до илеоцекального сфинктера.
Слизистая оболочка толстой кишки в норме выглядит бледной с хорошо видимыми кровеносными сосудами, блестящей, покрыта тонким слоем слизи, гаустрация выраженная, а циркулярные складки высокие, особенно в областях физиологических сфинктеров, где тонус циркулярных мышц кишки особенно высок (рис. 5.90). По ходу толстой кишки можно видеть полушаровидные образования размером до 0,5 см – подслизистые лимфоидные фолликулы.
С помощью колоноскопии проводится основная визуальная и морфологическая (биопсия) диагностика заболеваний толстой кишки, воспалительных, эрозивно-язвенных и опухолевых заболеваний (см. рис. 5. 30).
При воспалительных процессах в толстой кишке, особенно при язвенном колите изменения слизистой оболочки могут варьировать от умеренной гиперемии, петехий и умеренной кровоточивости до тяжелых патологических изменений (рыхлость, кровоточивость, отек, слизисто-гнойное отделяемое, наслоения фибрина, эрозии, язвы, рубцовые изменения, псевдополипы – язвенно-деструктивный колит) (см. рис. 5.22). Иногда сужение просвета кишки и псевдополипы трудно отличить от опухолевого поражения. В подобных случаях необходимо проведение биопсии.
При описании эндоскопической картины наиболее удобно использовать схему сегментарного строения пищевода по Бромбарту. Трахеальный (надаортальный) сегмент пищевода от его устья до дуги аорты (8 - 9 см). Аортальный сегмент равен диаметру дуги аорты (2,5 - 3 см). Бронхиальный сегмент — на уровне бифуркации трахеи. Аортально-бронхиальный сегмент - между нижним краем дуги аорты и верхним краем левого главного бронха. Подбронхиальный сегмент — от бифуркации трахеи до левого предсердия. Ретроперикардиальный сегмент располагается спереди от стенки левого предсердия до нисходящей аорты. Наддиафрагмальный сегмент занимает эпифренальное пространство (3 - 4см). Внутридиафрагмальный сегмент занимает область хиатуса, длиной около 2 см. Брюшной сегмент занимает нижнюю часть физиологической кардии (3 - 4 см).
Эзофагоскопическая картина в норме.
Вход в пищевод открывается в виде закругленного щелевидного отверстия, расположенного во фронтальной плоскости. Слизистая бледнорозового цвета, с тонким сосудистым рисунком, с нерезко выраженными продольными складками слизистой, которые при инсуффляции расправляются. Видны ритмичные циркулярные перистальтические сокращения стенок пищевода. Четко дифференцируется переход в желудок - кардия, где бледно-розовая слизистая пищевода меняется красноватой слизистой кардиального отдела желудка. При прохождении кардии ощущается легкое сопротивление.
Эндоскопическая семиотика пищевода.
Функциональные расстройства пищевода чаще выражены в гиперкинезии или гипокинезии.
Гиперкинезия пищевода выражается в усилении моторикн и тонуса стенок пищевода. Эндоскопическими находками при, гиперкинезии пищевода могут быть пищеводного отверстия диафрагмы, эзофагит, рефлюкс-эзофагит. При гиперкинезии отчетливо прослеживается поперечная складчатость слизистой пищевода.
Гипокинезия пищевода включает ослабление перистальтики и тонуса пищевода, зияние верхнего и нижнего сфинктеров пищевода. Эндоскопическая картина пептического эзофагита чаще соответствует его гипокинезии. Недостаточность кардии в эндоскопической практике встречается у 9,6% исследуемых пациентов. При пептическом эзофагите слизистая сглажена, лаково-красного цвета. В просвете пищевода виден рефлюксат из содержимого желудка.
Эзофагиты чаще наблюдаются в нижней части пищевода. Различные степени выраженности и распространения гиперемии и слизистой оболочки. Нередко видны воспалительные инфильтраты в виде отдельных участков. Слизистая оболочка покрыта беловатым или сероватым налетом, а при прогрессировании процесса - желтовато-серым фибринозным налетом, легко кровоточит.
Для эрозивного эзофагита характерно наличие неопределенной формы, чаще продольных эрозий, покрытых желто-серым налетом, легко снимающимся при эндоконтакте. Эрозивный эзофагит встречается чаще при рефлюкс эзофагите.
При фибринозном эзофагите слизистая оболочка беловато-серого цвета, мало смещаемая, стенки пищевода ригидны, При нагнетании воздуха пищевод с трудом расправляется, что сопровождается болезненными ощущениями. Рельеф слизистой неровный, кардиальное кольцо сомкнуто, складки грубые, отечные, утолщенные.
Для характеристики изменений в пищеводе при рефлюкс-эзофагите пользуются классификацией степеней изменения.
Степень (легкая форма): легкое покраснение и умеренно выраженный отек слизистой оболочки пищевода в нижней трети, чаще непосредственно над кардией и по задней стенке, широкие утолщенные складки, непостоянно зияющая кардия, желудочно-пищеводный рефлюкс, умеренное расширение пищевода в зоне воспаления, линия зет сохранена.
Степень (средней тяжести): выраженное покраснение и отек слизистой оболочки в нижней трети пищевода, расширение и утолщение складок, выраженное расширение в зоне воспаления. Легко кровоточит слизистая пищевода в зоне эзофагита при контакте с эндоскопом, кардия зияет, гастро-ззофагеальный рефлюкс. Сегментарный спазм пищевода в зоне эзофагита, линия зет почти не просматривается.
Степень (тяжелая форма): резкая гиперемия и отек слизистой в средней и нижней 1/3 пищевода. Слизистая покрыта легко снимающимся фибринозным налетом под которым нередко выявляются эрозированные или изъязвляющиеся кровоточащие участки. Чередующиеся расширение и спазм в зоне эзофагита, постоянно зияющая кардия. Желудочно-пищеводный рефлюкс. Линия зет (Z — линия) отсутствует.
Формы эзофагита: диспептический, смешанный, алгический Степени эзофагита: генерализованный, изолированные язвы, слияние поверхностных язв в сочетании с воспалением глубоких слоев стенки пищевода, фибринозный некроз - воспаление всех стенок пищевода.
Критерии эзофагита:
Диффузная гиперемия слизистой в виде продольных полос, гиперемия в нижней 1/3 делает незаметной Z-линию;
Наличие эрозии и язв;
Контактная и спонтанная кровоточивость слизистой;
Наличие гранулярных разрастании на слизистой, утолщение складок слизистой, недостаточное расправление стенок пищевода при инсуффляции;
Наличие лейкоплакий в пищеводе (гиперпластические разрастания покровного эпителия, количество слоев эпителия увеличивается в 5 - 6 раз, эпителиальные клетки приобретают кубическую форму).
Пептическая язва пищевода чаще является осложнением рефлюкс-эзофагита или аксиальной грыжи. Обычно язва вытянута по оси пищевода, неглубокая, дно покрыто белесоватым налетом. Вкрапления черного цвета указывают на бывшее кровотечение, а грязно-зеленый оттенок - на желчный рефлюкс. Слизистая отечна, гиперемирована, видны единичные эрозии. После заживления язвы происходит грубая деформация и структура пищевода. Рубец линейный или звездчатый.
Кандидомикоз пищевода в эндоскопической практике встречается крайне редко, но демонстративная эндоскопическая картина его не оставляет проблем в диагностике, кроме картины эзофагита видны «капли сметаны» в виде гладких или сморщенных очажков до 2 - 4 мм от белого до коричневого цвета, небольшие участки некроза и псевдомембранозные налеты.
Недостаточность кардии сопровождается и является причиной эзофагитов. Признаки недостаточности кардии: умеренное зияние ее, легкая расправляемость при инсуффляции, сглаженность рельефа слизистой кардиального жома, появление циркулярных складок, гастро-эзофагеальный рефлюкс.
Эндоскопические признаки аксиальной грыжи: укорочение расстояния от передних резцов до Z-линии, гастро-эзофагеальный рефлюкс, трансхиатальный пролапс слизистой желудка в пищевод, наличие рефлюксата в просвете пищевода, свободное прохождение аппарата через пролабирующий сегмент. Грыжевым мешком при аксиальной грыже является париетальная брюшина, грыжевым содержимым - желудок. Пример протокола: розетка кардии на расстоянии 35 - 36 см от передних резцов. Смыкание кардии отсутствует, слизистая пищевода в нижней трети отечна, складки утолщены. В грыжевом мешке желудочное содержимое и резко отечные и гиперемированные складки слизистой желудка, активна кровоточащие при эндоконтакте. Больной постоянно срыгивает воздух.
Варикозное расширение вен пищевода (ВРВП) чаще от одного до четырех стволов, от мелких извитых спавшихся вен до колбовидных, свисающих в просвет пищевода фрагментов вены. Бывают изолированные узлы или тотальное поражение вен пищевода. Пример: вход в пищевод овальной формы, свободно проходим. На фоне гладкой белесовато-розовой слизистой пищевода видны синеватые тяжи различной формы и диаметра, распластанные в подслизистом слое. Бывают единичные, сетевые, стволовые, смешанные формы ВРВП. Если есть выраженное воспаление при варикозном расширении вен пищевода - эндоскопию производить не следует.
Дивертикулы пищевода - мешковидные выпячивания, стенки пищевода, слепо заканчивающиеся. Дивертикулы пищевода различают врожденные и приобретенные, истинные (со всеми оболочками стенки пищевода) и ложные. По топографическим признакам различают: проксимальные фарингоэзофагеальные дивертикулы, эпибронхиальные и наддиафрагмальные дивертикулы. При явлениях дивертикулита ведущими симптомами являются: дисфагия, регургитация, дисфония, кашель, дурной запах изо рта. Показано оперативное лечение. Эндоскопически при дивертикуле: слизистая внутри гиперемирована, видны остатки пищи и слизи в мешке, он не полностью опорожняется, четко дифференцируются ворота дивертикула. В 10% дивертикулит осложняется эзофагитом.
Злокачественные опухоли пищевода
В 42% случаев злокачественные опухоли пищевода бывают в средней Уз, в 12% - 8 верхней 1/3, в 26% - в нижней 1/3 пищевода. Кардиоэзофагеальный рак встречается в 20%. По эндоскопической картине различают пять типов (по Штарку).
Ограниченная раковая инфильтрация (Штарк-1):
поражена одна стенка на ограниченном участке. При эндоскопии слизистая на этом месте бледна, отличается от окружающей, рельеф перестроен, складчатость отсутствует, перистальтика не прослеживается. По цвету ограниченный участок слизистой тусклый, при биопсии - фрагментация. Просвет пищевода не изменен.
Изъязвившийся рак пищевода (Штарк-2):
поражает одну или две стенки пищевода. Эндоскопически в виде язвы неправильной формы с нечеткими контурами, неглубоким дном покрытым фибрином. Воспалительный вал вокруг язвы отсутствует, просвет пищевода не изменен, перистальтики нет. При инструментальной пальпации края язвы ригидны.
Пристеночная опухоль (Штарк-3):
бляшковидный или полиповидный, на одной или двух стенках пищевода, бугристой формы, серовато-красного цвета. Суживает просвет пищевода. При пальпации - контактная кровоточивость. Консистенция может быть и мягкой. Перистальтика на участке опухоли не прослеживается.
Циркулярная раковая стриктура пищевода (Штарк-4):
просвет пищевода сужение 0,3 см. Стенка бугристая, серого цвета, каменной плотности, тусклая, умеренно кровоточит/при эндопальпацни и при биопсии.
Кардио-эзофагеальный рак пищевода (Штарк-5):
функция кардии всегда нарушается, что способствует забросу содержимого желудка в просвет пищевода. Линия зет нивелируется. Слизистая мелкозернистая, серого цвета, тусклая, ригидная, кровоточит. Дифференцировать с кардноспазмом.
Ранний рак пищевода поражает слизистый и подслизистый слои, распространяется до 5 см по длиннику пищевода. Верифицируется после . Чаще метастазов не бывает. Эндоскопические исследования и биопсия в 97% случаев позволяют выявить рак пищевода.
Инородные тела пищевода.
При инородных телах пищевода важно соблюдать последовательность в действиях, При подозрении инородного тела эндоскопическому исследований предшествует квалифицированная консультация . Эзофагоскопию следует производить в специализированном отделении (торакальном), чтобы, исключая последующую транспортировку больного, после исследования оказать и оперативную помощь в полном объеме. Нахождение инородного тела в пищеводе 4 - 5 суток приводит к локальным некрозам стенок пищевода. Чаще инородные тела застревают в устье пищевода или в грудном отделе. При рубцовых поражениях пищевода проксимальнее стриктуры застревают фрагменты пищи, образуя конгломерат (эзофаголитиаз). При извлечении инородных тел из пищевода необходимы осторожность и определенный опыт, т. к. перфорации стенки пищевода приводят к грозным осложнениям: периэзофагиту, подкожной эмфиземе, . Для эндоскопического удаления инородных тел используются: форцепты, петли, захваты типа «крокодил», «крысиные зубы», «тренога», вилочные и др. При извлечении инородных тел, вторгшихся в противоположные стенки пищевода, требуется тщательная визуальная оценка ситуации и крайняя осторожность при выведении в просвет тупого конца инородного тела (иглы). Затем игла извлекается из другой стенки. После этого, фиксируя край иглы одним из захватов извлекается инородное тело вместе с эндоскопом. Для объективной оценки степени повреждения стенок пищевода необходима эзофагоскопия после извлечения инородного тела.
Статью подготовил и отредактировал: врач-хирург- Powell J., McConkey C.C. The rising trend in oesophageal adenocarcinoma and gastric cardia. Eur J Cancer Prev 1992; 1: 265-269.
- Devesa S.S., Blot W.J., Fraumeni J.F. Changing patterns in the incidence of oesophageal and gastric carcinoma in the United States. Cancer 1998; 83: 2049-2053.
- Pohl H., Welch H.G. The role of overdiagnosis and reclassification incidence. J Natl Cancer Inst 2005; 97 (2): 142-146.
- Аксель Е.М., Давыдов М.И., Ушакова Т.И. Злокачественные новообразования желудочно-кишечного тракта: основные статистические показатели и тенденции. Совр онкол 2001; 3 (4): 36-59.
- Стилиди И.С., Сулейманов Э.А., Бохян В.Ю., Кононец П.В. Рак пищевода. Материалы Интернет-сайта Российского онкологического научного центра им. Н.Н. Блохина РАМН.
- Spechler S.J. Carcinogenesis at the gastroesophageal junction: free radicals at the frontier. Gastroenterology 2002; 122: 1518-1520.
- Moons L.M.G., Kusters J.G., van Delft J. et al. A pro-inflammatory IL-10/IL-12 gene profile is associated with an increased risk for developing Barrett"s esophagus . Gastroenterology 2006; 130 (4; Suppl 2): A76.
- Давыдов М.И., Тер-Ованесов М.Д., Стилиди И.С. Пищевод Баррета: от теоретических основ к практическим рекомендациям. Практич онкол 2003; 4 (2): 109-118.
- Barrett N.R. Chronic peptic ulcer of the oesophagus and "oesophagitis". Br J Surg 1950; 38: 175-182.
- Allison P.R., Johnstone A.S. The oesophagus lined with gastric mucous membrane. Thorax 1953; 8: 87-101.
- Giuli R., Siewert J.R., Couturier D., Scarpignato C. Barrett"s Esophagus. Paris: John Libbey Eurotext, 2003: 1-4.
- Spechler S.H., Sharma P., Souza R. et al. American Gastroenterological Association Medical Position Statement on the Management of Barrett"s Esophagus. Gastroenterology 2011; 140 (3): 1084-1091.
- Калинин А.В. Гастроэзофагеальная рефлюксная болезнь: диагностика, терапия, профилактика. Фарматека 2003; 7: 1-9.
- Locke G.R., Talley N.J., Fett S.L. et al. Prevalence and clinical spectrum of gastroesophageal reflux: a population based study in Olmsted County, Minnesota. Gastroenterology 1997; 112: 1448-1456.
- Cameron A.J., Zinsmeister A.R., Ballard D.J. et al. Prevalence of columnar lined Barrett"s esophagus. Comparison of population based clinical and autopsy findings. Gastroenterology 1995; 99: 918-922.
- Connor M.J., Weston A.P., Mayo M.S. et al. The prevalence of Barrett"s esophagus and erosive esophagitis in patients undergoing upper endoscopy for dyspepsia in a VA population. Dig Dis Sci 2004; 49: 920-924.
- Toruner M., Soykan I., Ensari A. et al. Barrett"s esophagus: prevalence and its relationship with dyspeptic symptoms. J Gastroenterol Hepatol 2004; 19: 535-540.
- Rex D.K., Cummings O.W., Shaw M. et al. Screening for Barrett"s esophagus in colonoscopy patients with and without heartburn. Gastroenterology 2003; 125: 1670-1677.
- Gerson L.B., Shetler K., Triadafilopoulos G. Prevalence of Barrett"s esophagus in asymptomatic individuals. Gastroenterology 2002; 123: 461-467.
- Azuma N., Endo T., Arimura Y. et al. Prevalence of Barrett"s esophagus and expression of mucin antigens detected by a panel of monoclonal antibodies in Barrett"s esophagus and esophageal adenocarcinoma in Japan. J Gastroenterol 2000; 35: 583-592.
- Lee J.I., Park H., Jung H.Y. et al. Prevalence of Barrett"s esophagus in an urban Korean population: a multicenter study. J Gastroenterol 2003; 38: 23-27.
- Ивашкин В.Т., Шептулин А.А., Трухманов А.С. и др. Рекомендации по обследованию и лечению больных гастроэзофагеальной рефлюксной болезнью (пособие для врачей). М 2001.
- Hirota W.K., Loughney T.M., Lazas D.J. et al. Specialized intestinal metaplasia, dysplasia and cancer of the esophagus and esophagogastric junction: prevalence and clinical data. Gastroenterology 1999; 116: 227-285.
- Lambert R., Hainaut P., Parkin D.M. Premalignant lesions of the esophagogastric mucosa. Semin Oncol 2004; 31: 489-512.
- Brittan M., Wright N.A. Gastrointestinal stem cells. J Pathol 2002; 197: 492-509.
- Wallner B., Sylvan A., Janunger K.G. et al. Immunohistochemical markers for Barrett"s esophagus and associations to esophageal Z-line appearance. Scand J Gastroenterol 2001; 36: 910-915.
- Takubo K., Honma N., Arai T. Multilayered epithelium in Barrett"s esophagus. Am J Surg Pathol 2001; 25: 1460-1461.
- Takubo K., Arai T., Sawabe M. et al. Structures of the normal esophagus and Barrett"s esophagus. Esophagus 2003; 1: 37-47.
- Moriya A., Grant J., Mowat C. et al. In vitro studies indicate that acid catalysed generation of N-nitrosocompounds from dietary nitrate will be maximal at the gastro-oesophageal junction and cardia. Scand J Gastroenterol 2002; 37: 253-261.
- Кашин С.В., Иваников И.О. Пищевод Баррета: принципы эндоскопической диагностики и медикаментозной терапии. Рос журн гастроэнтерол гепатол колопроктол 2006; 6: 73-78.
- Lambert R., Sharma P. Paris Workshop on Columnar Metaplasia. Endoscopy 2005; 37 (9): 879-920.
- Wallner B., Sylvan A., Janunger K.G. Endoscopic assessment of the "Z-line" classification among endoscopists. Gastrointestinal Endoscopy 2002; 55: 65-69.
- Sharma P., Dent J., Armstrong D. et al. The development and validation of an endoscopic grading system for Barrett"s esophagus: the Prague C & M criteria. Gastroenterology 2006; 131 (5): 1392-1399.
- Василенко В.Х., Гребенев А.Л. Грыжи пищеводного отверстия диафрагмы. М: Медицина 1978; 59-68.
- Ragunath K., Krasner N., Raman V.S. et al. A Randomized, Prospective Cross-Over Trial Comparing Methylene Blue-Directed Biopsy and Conventional Random Biopsy for Detecting Intestinal Metaplasia and Dysplasia in Barrett"s Esophagus. Endoscopy 2003; 35 (12): 998-1003.
- Kashin S., Nadezhin A., Agamov A. et al. High-magnification endoscopy improves detection of specialized intestinal metaplasia in patients with GERD. Abstracts 13th UEGW. Gut 2005; 54 (Suppl 7): A54.
- Curvers W., van den Broek F., Reitsma J. et al. Systematic review of narrow-band imaging for the detection and differentiation of abnormalities in the esophagus and stomach. Gastrointestinal Endoscopy 2009; 69 (2): 307-317.
- Yousef F., Cardwell C., Cantwell M. et al. The Incidence of Esophageal Cancer and High-Grade Dysplasia in Barrett"s Esophagus: A Systematic Review and Meta-Analysis. Am J Epidemiol 2008; 168 (3): 237-249.
- Sampliner R.E. Practice Parameters Committee of the American College of Gastroenterology. Updated guidelines for the diagnosis, surveillance, and therapy of Barrett"s esophagus. Am J Gastroenterol 2002; 97 (8): 1888-1895.
- Narrow Band Imaging (NBI) vs High-Magnification Chromoendoscopy(HMC) in Detection and Endoscopic Surveillance of Barrett"s Esophagus (BE). S. Kashin, A. Nadezhin, A. Agamov, I. Politov, V. Goncharov, E. Rassadina, I. Kislova, D. Zavyalov, E. Velikanova. Abstracts 14th UEGW, Gut Endoscopy 2006; 38 (Suppl): A33.
- Kashin S., Zakrevskaya E., Ivanikov I. et al. Types of Mucosal Patterns in Barrett"s Esophagus (BE): Correlation Between High-Magnification Endoscopy (HME) with Narrow Band Imaging (NBI) and Histology. Gastrointestinal Endoscopy 2009; 69 (5): AB368.
- van Pinxteren B., Numans M.E., Bonis P.A. et al. Short-term treatment with proton pump inhibitors, H2-receptor antagonists and prokinetics for gastro-oesophageal reflux disease-like symptoms and endoscopy negative reflux disease. Cochrane Database System Review 2000; 2.
- Peters F.T., Ganesh S., Kuipers E.J. et al. Endoscopic regression of Barrett"s esophagus during omeprazole treatment: a randomised doble blind study. Gut 1999; 45: 489-494.
- Triadafilopoulos G. Proton pump inhibitors for Barrett"s oesophagus Gut 2000; 46; 144-146.
- Klinkenberg-Knol E.C., Nelis F., Dent J. et al. Long-term omeprazole treatment in resistant gastroesophageal reflux disease: efficacy, safety and influence on gastric mucosa. Gastroenterology 2000; 118: 661-669.
- Wetscher G.J., Gadenstaetter M., Klingler P.J. et al. Efficacy of medical therapy and antireflux surgery to prevent Barrett"s metaplasia in patients with gastroesophageal reflux disease. Ann Surg 2001; 234: 627-632.
- Hillman L.C., Chiragakis L., Shadbolt B. et al. Proton-pump inhibitor therapy and the development of dysplasia in patients with Barrett"s esophagus. Med J Aust 2004; 180: 387-391.
- Sagar P.M., Ackroyd R., Hosie K.B. et al. Regression and progression of Barrett"s esophagus after antireflux surgery. Br J Surg 1990; 49: 537.
- Seewald S., Akaraviputh T., Seitz U. et.al. Circumferential EMR and complete removal of Barrett"s epithelium: a new approach to management of Barrett"s esophagus containing high-grade intraepithelial neoplasia and intramucosal carcinoma. Gastrointest Endosc 2003; 57 (7): 854-859.
- Soehendra N., Seewald S., Groth S. et al. Use of modified multiband ligator facilitates circumferential EMR in Barrett"s esophagus (with video). Gastrointest Endosc 2006; 63 (6): 847-852.
- Deviere J. Thermal Endoscopic Therapy of Barrett"s esophagus. In Barrett"s esophagus and Esophageal Adenocarcinoma. Eds: Sharma P., Sampliner R. Blackwell Publishing 2006; 188-195.
- Seewald S., Ang T.L., Gotoda T., Soehendra N. Total endoscopic resection of Barrett esophagus. Endoscopy 2008; 40 (12): 1016-1020.
- Sharma P. Barrett"s Esophagus. N Engl J Med 2009; 361: 2548-2556
Обследованы 274 пациента с подтвержденным эрозивным эзофагитом без гистологических признаков пищевода Баррета (ПБ). Установлены характерные эндоскопические и морфологические признаки эзофагита и динамика изменений слизистой пищевода после проведения медикаментозной терапии ингибиторами протонной помпы, Н 2 -блокаторами и комбинированными антацидами.
Changes in the mucosa of the esophagus with gastroesophageal reflux disease under the influence of medical therapy
The study included 274 patients with confirmed erosive esophagitis without histological signs of Barrett’s esophagus. Characteristic endoscopic and morphological features of esophagitis and dynamics of esophageal mucosal change after drug therapy using proton pump inhibitors, H2 blockers and antacids combined were presented.
Все возрастающая актуальность проблемы гастроэзофагеальной рефлюксной болезни (ГЭРБ) связана с ростом числа больных с этой патологией во всем мире. Проводящиеся в мире многочисленные эпидемиологические исследования свидетельствуют о том, что распространенность ГЭРБ сохраняется стабильно высокой на протяжении последних десятилетий — ею страдает до 40-50% взрослого населения . По данным одного из последних популяционных эпидемиологических исследований, проведенного в России в рамках реализации программы МЭГРЕ (Многоцентровое исследование «Эпидемиология гастроэзофагеальной рефлюксной болезни в России»), частота ГЭРБ (наличие изжоги и/или кислой отрыжки 1 раз/нед. и чаще на протяжении последних 12 месяцев) составляет 13,3% населения .
ГЭРБ, эзофагит и метаплазия пищевода (пищевод Баррета (ПБ)) представляют последовательность событий, которые создают предпосылки для развития аденокарциномы пищевода (АП). Распространенность ПБ среди лиц с эзофагитом приближается к 8% с колебаниями в диапазоне от 5 до 30% . Он выявляется у 6-12% лиц, которым проводится эндоскопическое исследование. Большое количество пациентов, длительно принимающих самостоятельно различные медикаментозные средства (антацидные препараты, блокаторы Н 2 -рецепторов, ингибиторы протонной помпы (ИПП), а также пациенты с асимптоматичной формой ГЭРБ не обращаются к врачам, а следовательно, наличие ПБ у них не может быть установлено. Неудивительно, что данные о распространенности ПБ по результатам исследования аутопсийного материала значительно различались. Распространенность ПБ по результатам аутопсии оказалась в 16 раз выше частоты клинически диагностированных случаев. Это свидетельствует о том, что ПБ — достаточно распространенное состояние, которое в большинстве случаев остается невыявленным.
ПБ рассматривается в последние годы как предраковое состояние. Повышение частоты развития аденокарциномы нижней трети пищевода связывают именно с ПБ. Под ПБ подразумевают выстилку слизистой оболочки нижней трети пищевода не многослойным плоским, а цилиндрическим эпителием и появление в основе железистых структур желудочного или кишечного типа.
Для диагностики ПБ необходимы визуализация дистального сегмента пищевода и выявление цилиндрического эпителия и наличие кишечной метаплазии с гистологическим подтверждением. Выделяют три варианта цилиндрической метаплазии эпителия: кардиальный желудочный, фундальный желудочный и специализированный кишечный с бокаловидными клетками . Необходимо подчеркнуть, что из трех вариантов цилиндрического эпителия, обнаруживаемых при ПБ, именно последний обладает наибольшим злокачественным потенциалом , предрасполагает к АП и повышает риск ее возникновения в 30-125 раз. Поэтому необходимо раннее выявление пациентов с ПБ.
Основными задачами исследования являлись:
— определить анатомические и функциональные предпосылки поражения дистального сегмента пищевода;
— определить характерные эндоскопические признаки эзофагита и степень их выраженности;
— определить морфологические изменения в зоне поражения слизистой пищевода;
— определить динамику изменений слизистой пищевода после проведения медикаментозной терапии.
Материал и методы. За 1999-2006 года в лечебно-диагностическом центре проведено более 22 000 эндоскопических исследований. Эндоскопические исследования проводили эндоскопами GIF-40, GIF-160, ЛОМО. Макроскопически эрозивный эзофагит выявлялся у 38% пациентов. С 1999 по 2002 года применялась эндоскопическая классификация Савари и Миллера (Savary-Miller, 1977), с 2003 года степень эрозивного эзофагита оценивалась по Лос-Анджелесской классификации. В исследуемую группу были включены пациенты, у которых при первичной эндоскопии верхних отделов пищеварительной системы обнаруживалась ГЭРБ с эрозивным эзофагитом. У всех больных при включении был гистологически исключен ПБ.
Под наблюдением находилось 274 пациента с ГЭРБ на стадии эрозивного эзофагита, которые получали комплексную медикаментозную терапию. 1-я группа (157 больных) получала ИПП по схеме — 20мг/сут. 14 дней и поддерживающая доза 10мг/сут. до 12 недель. 2-я группа (117 пациентов) получала Н 2 -блокаторы по 0,04 г 1 раз в сутки перед сном или по 0.02 г 2 раза в сутки и комбинированные антациды (альмагель, маалокс и т.п.). Выделение группы, принимающей Н 2 -блокаторы, было определено тем, что набор больных был начат в 1999 году, когда применение ИПП при ГЭРБ не было распространенным.
Эндоскопическое исследование верхних отделов проводилось в начале обследования, на 4-й неделе и на 12-й неделе. С целью визуализации измененных участков слизистой пищевода использовали раствор Люголя и метод обратимой денатурации (обработка слизистой 1,5-3% уксусной кислотой).
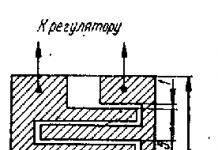
Биопсия пищевода в начале наблюдения и на 12-й неделе . Для достоверной диагностики состояния пищевода брали не менее 4 биоптатов на 2 и более сантиметров проксимальнее Z-линии, так как анатомическая зона пищеводно-желудочного перехода не совпадает с таковой, выявляемой эндоскопически (рис. 1).
Рисунок 1. Анатомическая и фактическая Z-линия
Результаты и обсуждение
При первичной эндоскопии оценивалась степень выраженности эзофагита, характер поражения пищевода представлен в таблице 1.
Таблица 1
Эндоскопическая степень активности эрозивного эзофагита
Кроме определения степени ГЭРБ мы также оценивали наличие грыжи пищеводного отверстия диафрагмы (ГПОД), наличие пролапса слизистой желудка в просвет пищевода (пролапс слизистой желудка в просвет пищевода более 3,0 см мы расценивали как скользящую грыжу). Детально оценивали состояние слизистой пищевода над кардиальным жомом. Под кардиальным жомом мы понимаем пищеводно-желудочный переход. Особое внимание уделяли состоянию перехода многослойного эпителия пищевода в цилиндрический эпителий желудка. Граница между однослойным цилиндрическим эпителием желудка и многослойным плоским эпителием пищевода- Z-линия, в норме чаще располагающаяся на границе пищевода и желудка, у некоторых больных несколько «смещается» в проксимальном направлении (рис. 2).
Рисунок 2. Различные положения Z-линии относительно кардиального жома
 Биопсию проводили как при выявлении эрозивных изменений слизистой, так и при всех эндоскопических изменениях отличных от нормы:
Биопсию проводили как при выявлении эрозивных изменений слизистой, так и при всех эндоскопических изменениях отличных от нормы:
— визуализация сосудистого рисунка в виде параллельных линий;
— нерегулярность Z-линии;
— очаговое изменение окраски слизистой и отсутствие сосудистого рисунка в нижней части пищевода;
— гипертрофические разрастания (белая полоса выступающей слизистой без сосудистого рисунка, полиповидные образования и складки, треугольные выступы, утолщение Z-линии и т.п.).
При эндоскопическом исследовании провоцируется рвотный рефлекс, что приводит к пролапсу слизистой оболочки желудка в пищевод (рис. 3). В данном случае говорить об эндоскопических признаках недостаточности кардии и особенно о ГПОД следует с большой осторожностью.
Рисунок 3. Транскардиальная миграция слизистой оболочки (пролапс)
 Для эндоскопического диагноза скользящих ГПОД необходимо сочетание следующих анатомических и функциональных признаков: 1) уменьшения расстояния от передних резцов до кардии; 2) наличия грыжевой полости (рис. 4); 3) наличия «второго входа» в желудок (рис. 4); 4) зияние кардии или неполного ее смыкания (рис. 5); 5) транскардиальных миграций слизистой оболочки (пролапсы — релапсы); 6) гастроэзофагеальных рефлюксов содержимого желудка; 7) признаков грыжевого гастрита и рефлюкс-эзофагита. Эти симптомы видны более отчетливо при фиксированных ГПОД, а также при больших грыжах II-III степени.
Для эндоскопического диагноза скользящих ГПОД необходимо сочетание следующих анатомических и функциональных признаков: 1) уменьшения расстояния от передних резцов до кардии; 2) наличия грыжевой полости (рис. 4); 3) наличия «второго входа» в желудок (рис. 4); 4) зияние кардии или неполного ее смыкания (рис. 5); 5) транскардиальных миграций слизистой оболочки (пролапсы — релапсы); 6) гастроэзофагеальных рефлюксов содержимого желудка; 7) признаков грыжевого гастрита и рефлюкс-эзофагита. Эти симптомы видны более отчетливо при фиксированных ГПОД, а также при больших грыжах II-III степени.
Рисунок 4. Грыжевая полость и наличие «второго» входа в желудок
Рисунок 5. Зияние кардии
 При проведении эндоскопии нами были выделены анатомо-функциональные нарушения (табл. 2), которые у части больных сочетались между собой. Наиболее частым изменением являлся гастродуоденальный рефлюкс.
При проведении эндоскопии нами были выделены анатомо-функциональные нарушения (табл. 2), которые у части больных сочетались между собой. Наиболее частым изменением являлся гастродуоденальный рефлюкс.
Таблица 2
Эндоскопические выявленные анатомо-функциональные нарушения
При контрольной эзофагогастроскопии через 12 недель в 1-й группе полное заживление эрозивных изменений слизистой пищевода произошло у 64,9% (102 пациента), во 2-й группе — у 60,7% (71 пациент).
У всех больных проводилось морфологическое исследование биоптатов пищевода.
Вариантами гистологического заключения являлись разные степени воспаления, воспалительно-дистрофические изменения, метапластические изменения и дисплазия эпителия.
Приводим обобщенные морфологические данные.
Чаще выявлялись атрофия эпителия, истончение эпителиального слоя, но изредка наряду с атрофией были обнаружены участки гипертрофии эпителиального пласта. В отдельных случаях дистрофия завершалась некрозом кератиноцитов, особенно ярко выраженном в поверхностных слоях эпителия. Базальная мембрана эпителия сохраняла обычные размеры, но у некоторых больных была утолщена и склерозирована.
Наряду с выраженными дистрофически-некротическими изменениями эпителия отмечалась гиперемия сосудов, во всех случаях количество сосочков было значительно увеличено. В толще эпителия и в субэпителиальном слое выявлялись очаговые (как правило, периваскулярные), а местами диффузные лимфоплазмоцитарные инфильтраты с примесью единичных эозинофилов и полинуклеарных нейтрофилов. Инфильтраты располагались как в области сосочков, так и в более глубоких слоях под эпителием, при этом отмечалось разволокнение мышечных волокон. В отдельных случаях длительно текущего заболевания среди воспалительных инфильтратов были обнаружены сосуды с явлениями продуктивного васкулита. Инфильтрат, как правило, был чрезвычайно полиморфный, доминировали моноциты, плазматические клетки, лимфоциты, макрофаги, а при длительно текущем эзофагите — фибробласты. При активно текущем эзофагите количество нейтрофилов оказывалось значительным, при этом часть нейтрофилов обнаруживалась в толще эпителиального пласта внутри клеток (лейкопедез эпителия).
У части больных явлений активно текущего воспаления гистологически не обнаруживалось. При этом в слизистой оболочке пищевода отмечалось разрастание рыхлой, а местами плотной волокнистой соединительной ткани (склероз). В полях склероза нередко встречались фибробласты и разрушенные макрофаги. Гладкомышечные клетки собственной пластинки слизистой оболочки демонстрировали явления выраженной дистрофии или атрофии, а в редких случаях состояние коагуляционного некроза. В отдельных случаях клетки нижней трети эпителиального пласта оказывались полиморфными, с умеренно гиперхромными ядрами, в единичных клетках наблюдались фигуры митозов. Подобные изменения были характерны для слабо выраженной дисплазии эпителия.
При гистологическом исследовании была выявлена метаплазия плоского неороговевающего эпителия пищевода, которая приводила к появлению цилиндрического эпителия с фундальными железами (выявлялись париетальные, главные и добавочные клетки в железах). При этом железы были немногочисленны, сдавлены разрастаниями соединительной ткани и диффузным лимфоплазмоцитарным инфильтратом.
Если метаплазия приводит к появлению цилиндрического эпителия кардиального или фундального типа слизистой желудка, то риск развития аденокарциномы пищевода не увеличивается. Однако, если метаплазия (неполная кишечная) приводит к появлению специализированного цилиндрического эпителия, риск озлокачествления становится явным .
На 12-й неделе морфологически подтвержденный ПБ, а именно — изменение слизистой пищевода в виде кишечной метаплазии, был выявлен у 8% пациентов (22). В 1-й группе ПБ выявлен у 11,4% (18 больных). Во 2-й группе ПБ выявлен у 3,4% (4 пациента) (табл. 3).
Таблица 3
Частота выявления ПБ через 12 недель
1-я группа — 157 пациентов | 11,46% (18 пациентов) |
2-я группа — 117пациентов | 3,4% (4 пациента) |
Всего 274 (100%) | 8 % (22 пациента) |
ПБ на коротком отрезке (меньше 3 см) выявлен у 19 больных, на длинном отрезке — у 3 пациентов. Было выявлено 2 пациента с дисплазией I-II степени.
Интересно отметить частоту сочетания ПБ и анатомо-функциональных нарушений:
— ГПОД — 7 пациентов,
— пролапс слизистой желудка в просвет пищевода — 14 пациентов,
— гастроэзофагеальный рефлюкс — 1 пациент.
Заключение
В настоящее время известно, что достоверных клинических проявлений ПБ не существует. Однако установлено, что имеются определенные факторы риска: мужской пол, возраст старше 45 лет, курение, изжога в анамнезе в течение нескольких лет, эпизоды ночной изжоги, избыточный вес. Эти пациенты, вероятно, нуждаются при проведении эндоскопического исследования верхних отделов пищеварительного тракта для прицельного исключения ПБ. Также одним из эндоскопических маркеров ПБ могут являться анатомо-функциональные нарушения.
Основой ведения ПБ является активное диспансерное наблюдение для возможности предупреждения развития АП. Одним из основных является проведение гистологического исследования. Взятие биоптатов проводится из 4 участков метаплазированной слизистой оболочки. При выявлении ПБ необходим тщательный поиск диспластических изменений. Если дисплазия не обнаружена, рекомендуется динамическое наблюдение с проведением эндоскопического исследования каждый год. Если присутствует дисплазия низкой степени, необходима консервативная терапия. При исчезновении диспластических изменений повторное эндоскопическое исследование проводят через год. При сохранении дисплазии и увеличении степени диспластических изменений целесообразна оценка этих изменений еще одним специалистом-гистологом. В случае подтверждения дисплазии высокой степени продолжение только эндоскопического наблюдения нецелесообразно, необходима более активная тактика или эндоскопическая резекция слизистой пищевода или хирургическое вмешательство.
М.Ф. Самигуллин, Д.И. Абдулганиева
Казанская государственная медицинская академия
Казанский государственный медицинский университет
Самигуллин Марсель Фаикович — кандидат медицинских наук, заведующий лечебно-диагностическим центром Госпиталя ветеранов войны
Литература:
1. Маев И.В., Самсонов А.А., Одинцова А.Н. и др. Динамика показателей качества жизни больных гастроэзофагеальной рефлюксной болезнью на фоне сочетанной терапии. РМЖ 2010; 5: 283-288.
2. Лазебник Л.Б., Машарова А.А., Бордин Д.С. и др. Многоцентровое исследование «Эпидемиология гастроэзофагеальной рефлюксной болезни в России (МЭГРЕ): первые итоги. Экспериментальная и клиническая гастроэнтерология 2009; 6: 4-12.
3. Ивашкин В.Т., Трухманов А.С. Современный подход к терапии гастроэзофагеальной рефлюксной болезни во врачебной практике. РМЖ 2003; 2: 43-48.
4. Е.В. Онучина. Возможности терапевтического ведения больных с пищеводом Барретта. Сибирский медицинский журнал 2008; 5: 9-12.
5. Мозговой С.И., Яковлева Э.В., Лининг Д.А., Кононов А.В. Кишечная метаплазия слизистой оболочки желудка: классификация, методика детекции и сложности гистопатологической интерпретации с позиции современной практической гистохимии. эксперим. и клин. гастроэнтерол. 2004; 1 (внеочередной вып.): 114-125.
Эзофагоскопия является одним из наиболее достоверных методов исследования, позволяющих изучить слизистую оболочку пищевода и желудка на основании данных визуального осмотра, а также результатов гистологического и цитологического изучения биопсийного материала, полученного прицельно через эндоскоп. Следует отметить, что визуально можно выявлять лишь относительно большие грыжи пищеводного отверстия диафрагмы. Использование фиброэзофагогастроскопии при hiatus hernia больше оправдано для диагностики рефлюкс-эзофагита (Григорьев П.Я. и соавт., 1990,1996). Сочетание ряда признаков при эндоскопическом исследовании позволяет говорить о наличии хиатальной грыжи у больного. Этими признаками являются: уменьшение расстояния от резцов до пищеводно-желудочного перехода, наличие грыжевых ворот, обнаружение "воронки" при ретроградном осмотре кардии, пролапс слизистой желудка в пищевод (Кубышкин В.А., Корняк Б.С, 1999).
\г В своей работе мы выделяем несколько эндоскопических признаков грыжи пищеводного отверстия диафрагмы.
При эндоскопическом исследовании отмечаются различные стадии воспалительного процесса от катарального до язвенно-некротического эзофагита, наиболее выраженные в нижней трети пищевода. Обычно нормаль-
- -кольцо " А " - мышечное кольцо; 2 - кольцо " Б " - хиатальное сужение пищевода; 3 - грыжевая полость; 4 - "второй вход" в желудок
ной резистентности диафрагмального кольца не ощущается, и эзофагоскоп проваливается в желудок. Можно наблюдать затекание желудочного содержимого в пищевод из желудка.
Гистологически рефлюкс-эзофагит характеризуется воспалительной инфильтрацией подслизистого слоя преимущественно плазмоцитами, нейтрофильны- ми лейкоцитами и лимфоцитами, отеком слизистого и подслизистого слоев, вакуольной дистрофией и окантозом эпителия. Наряду с этим выявляются склеротические и кистозные изменения в слизистой оболочке, десквамация и складчатость эпителия, венозный застой, микрогематомы. Об эзофагите свидетельствуют изменения хотя бы одного биоптата.
Для унификации и оценки данных эндоскопического исследования используют классификацию степени выраженности эзофагита по Savary-Miller, при этом различают четыре стадии заболевания:
- стадия - округлые и продольные поражения, которые не сливаются и распространяются от Z-линии к слизистой оболочке пищевода (рис. 11);
- стадия - сливающиеся транзиторные поражения в зоне Z-линии, не захватывающие всю поверхность слизистой оболочки (рис. 12);
- стадия - язвенные поражения, сливающиеся в нижней части пищевода и охватывающие всю поверхность слизистой оболочки (рис. 13);
- стадия - хронические язвенные поражения пищевода, фиброзный стеноз, укорочение пищевода (пищевод Барретта) (рис. 14).


у 6,5% и эзофагит 4 степени (пищевод Баррета) - у 1% пациентов (классификация по Savary-Miller). Подозрение на наличие хиатальной грыжи возникло у 67,3% больных. Язвенная болезнь двенадцатиперстной кишки диагностирована у 42,9% больных в 1 группе (открытая фундопликация по Nissen), 39,3% - во второй (лапароскопическая фундопликация по Nissen), в 17% и 34,4% случаев в 3-й (задняя парциальная фундопликация по Toupet) и 4-й (2-х сторонняя фундопликация по Toupet) группах соответственно.
На сегодняшний день в связи с изменениями концепции о пищеводе Барре- та следует остановиться на его определении и диагностике.
В настоящее время считается, что пищевод Баррета - это приобретенное состояние, возникающее в результате хронического повреждения слизистой оболочки дистального отдела пищевода за счет рефлюкса, при котором цилиндрический железистый эпителий, имеющий в своем составе специализированные метаплазированные по кишечному типу клетки, замещает многослойный плоский эпителий в дистальном отделе пищевода, независимо от длины мета- плазированного участка. Синонимом понятия "пищевод Баррета"является "цилиндрическая метаплазия слизистой пищевода" (Dent J. и соавт.,1991; Armstrong D. и соавт., 1992; Кубышкин В.А., Корняк Б.С, 1999). При эндоскопическом исследовании должен быть заподозрен пищевод Баррета, если переход плоскоклеточного эпителия в цилиндрический (Z-линия) не совпадает с положением кардии. Граница может быть четкой и ровной, однако чаще имеет вид пальцевидных выпячиваний.
Поскольку эндоскопические признаки цилиндрической метаплазии слизистой пищевода по кишечному типу могут отсутствовать, биопсия берется из 4 выбранных наугад точек г.о окружности пищевода с интервалом в 1-2 см по всей длине сегмента (Кубышкин В.А., Корняк Б.С, 1999). Диагноз ставится на
основании данных эндоскопии с биопсией, что дает возможность выявить кишечную метаплазию слизистой дистального отдела пищевода.