Существует огромное количество классификаций теорий старения, исследователи выделяют множество групп- теории программированного старения, стохастические (вероятностные), молекулярно-генетические, нейроэндокринные и многие другие. Разделение это весьма условно, т.к. теории должны охватывать все механизмы, задействованные в процессе старения. Механизмы старения достаточно сложны и многообразны. Сегодня существует несколько альтернативных теорий, которые отчасти противоречат друг другу, а отчасти – дополняют. Сейчас научный мир все больше интересуется проблемой старения, созданы институты по этой проблеме, исследовательские группы и т.д. Накапливается огромный объем данных и, может быть уже очень скоро процесс старения будет разгадан.
Рассмотрим теории старения в порядке, данном в знаменитой монографии Бена Беста "Механизмы старения 2006 года. Больше информации об известном можно найти на его персональном сайте .
Эволюционная теория и видо-специфичное старение
 Эта теория зародилась когда Рассел Уоллес(Russell Wallace), знаменитый эволюционист, работавший с Дарвином, выдвинул идею о том, что долголетие, превышающее возраст потомства невыгодно для видов. Дети и родители конкурируют за ресурсы. Это может свидетельствовать в пользу идеи о генетически- программируемом старении
. Дополнительным аргументом является программируемое кортикостероид-опосредованное саморазрушение лосося после нереста. Но как заметил биолог Герман Медавар (Herman Medawar), если бы не было старения, то не было бы необходимости в размножении.
Эта теория зародилась когда Рассел Уоллес(Russell Wallace), знаменитый эволюционист, работавший с Дарвином, выдвинул идею о том, что долголетие, превышающее возраст потомства невыгодно для видов. Дети и родители конкурируют за ресурсы. Это может свидетельствовать в пользу идеи о генетически- программируемом старении
. Дополнительным аргументом является программируемое кортикостероид-опосредованное саморазрушение лосося после нереста. Но как заметил биолог Герман Медавар (Herman Medawar), если бы не было старения, то не было бы необходимости в размножении.
Если старение- продукт действия сил эволюции, то оно должно быть программируемым. Но большая часть животных в природе гибнет от несчастных случаев, конфликтов и болезней, и в этих условиях кажется сомнительным, что старение предопределено эволюцией. С другой стороны- уже на ранних стадиях старения снижается способность животного выжить, таким образом происходит селекция против старых особей.
Представители альтернативной точки зрения сравнивают генетическое программирование с конструированием спутника для сбора информации о планете. Конструирование сконцентрировано на том, чтобы гарантировать, что спутник достигнет места назначения и представит собранные данные когда облетит планету. Аналогия очень образная, под спутником подразумевается репродуктивный период. Одной из целей репродукции является разрушение особи.
Широкий диапазон продолжительности жизни разных видов кажется убедительным доказательством того, что старение генетически предопределено. Слон живет в 10-20 раз дольше, чем мышь, но число сердцебиений у них одинаковое в течение жизни, просто у слона 30 в минуту, а у мыши 300. Оба вида делают 200 млн. дыхательных движений. Оба имеют метаболический потенциал около 200 ккал (он характерен и для других млекопитающих, но у человека он равен приблизительно 800ккал- мозг использует больше энергии, чем любой другой орган). Геронтологи, которые сравнивали продолжительности жизни различных видов, объясняют это противоречие тем, что корреляция продолжительности жизни и веса гораздо лучше, чем корреляция с массой мозга у приматов.
Значимые характеристики вида также влияют на продолжительность жизни у разных видов: большой размер, способность летать, мозг, наличие иголок, раковины или панциря, холоднокровность. Все, кроме последней характеристики, снижает уязвимость для хищников.
Конкуренция особей одного вида за партнеров и ресурсы более важна, чем хищники и другие опасности. Эволюционные силы позволяют развиваться более сильным и устойчивым животным, это подразумевает и оставление как можно большего числа потомков, и каждый потомок должен получать больше заботы и ресурсов. Выживание генов лучше обеспечивается увеличением продолжительности жизни и репродуктивного периода "репродуктивно-успешных" взрослых особей, у которых будет больше потомства, значительное число которых не выживет и не станет репродуктивно-активными особями.
Коротко-живущие организмы растрачивают метаболическую энергию на антиоксиданты и репарацию ДНК вместо того, чтобы использовать ее для роста и репродукции. Когда у животного есть враги, то эволюция вкладывает некоторые ресурсы в быструю репродукцию и репарацию (в том числе и репарацию ДНК), а большее количество генетических ресурсов в удлинение репродуктивного периода (а значит удлиняется и продолжительность жизни). Например, у птиц мембрана митохондрий содержит большое количество ненасыщенных жирных кислот, что делает их менее уязвимыми для перекисного окисления. Белковый комплекс дыхательной цепи митохондрий генерирует у птиц меньше , чем у млекопитающих. Это свидетельствует о том, что животные с хорошо сконструированными клетками могут жить несколько столетий
. Человеческие стволовые клетки теоретически могут жить миллионы лет благодаря усиленной продукции ферментов ДНК- репарации, антиоксидантных ферментов и теломеразы.
 Эволюционные биологи проводят эксперименты по искусственной селекции для определения роли эволюции в детерминации продолжительности жизни. Подобные исследования проводит Майкл Роуз (Michael Rose) из Department of Ecology and Evolutionary Biology , University of California. В своих работах он исследовал многие поколения дрозофил и определил, что те особи, которые оставляют потомство в конце жизненного цикла, живут на 30% дольше других. Нагрузка при увеличенной продолжительности жизни определяет повышенный уровень SOD, CAT и ксантиндегидрогиназы, а также белков теплового шока, это увеличивает сопротивляемость стрессу. Например, экспрессия Hsp22 (одного из белков теплового шока) у долгоживущих особей в 2-10 раз выше.
Эволюционные биологи проводят эксперименты по искусственной селекции для определения роли эволюции в детерминации продолжительности жизни. Подобные исследования проводит Майкл Роуз (Michael Rose) из Department of Ecology and Evolutionary Biology , University of California. В своих работах он исследовал многие поколения дрозофил и определил, что те особи, которые оставляют потомство в конце жизненного цикла, живут на 30% дольше других. Нагрузка при увеличенной продолжительности жизни определяет повышенный уровень SOD, CAT и ксантиндегидрогиназы, а также белков теплового шока, это увеличивает сопротивляемость стрессу. Например, экспрессия Hsp22 (одного из белков теплового шока) у долгоживущих особей в 2-10 раз выше.
Статьи доктора Роуз:
Отсроченное старение и сопротивляемость обезвоживанию у Drosophila melanogaster.
К сожалению такие разносторонние исследования проводятся на лабораторных моделях, которыми давно стали дрозофилы. Подобные исследования на людях сильно затруднены в силу биологических причин- невозможно в полной мере проследить столько поколений людей.
Если говорить о теории, то мало конкретизирована и представляет обобщение других теорий (хотя появилась раньше, чем другие), например свободнорадикальной теории, теломеразной и др.
Однако, как отмечалось выше, есть и противники этой теории. Среди них Рендольф Хаус (Randolph Howes) и Энтони Линнен (Anthony Linnane), который в свое время был ярым ее сторонником, но потом пересмотрел свои взгляды. Howes в 2006 году выпустил монографию "Свободнорадикальная фантазия: богатство парадоксов" . Исследователи отдают должное роли этой теории в ситории, но отмечают в ней некоторые ошибки. Так, они считают, что оценка уровня свободных радикалов завышена, известны и эффективно работают системы репарации, свободные радикалы участвуют в выработке энергии и регуляции клеточного метаболизма, гомеостаза. Широкое использование антиоксидантов не помогает в борьбе с пандемиями онкологических заболеваний, диабета, сердечно-сосудистых заболеваний и старением.
В любом случае, в свободнорадикальной теории есть рациональное зерно, но остается много неразрешенных вопросов:
1) почему,если теория верна, антиоксиданты неэффективны?
2) как можно защитить клетку и организм вцелом от оксидативного стресса?
3) как активизировать внутренние резервы?
4) как определить тот лимит, после которого возникает рак, диабет, атеросклероз и прочие спутники старения?
Ждем ответов от исследователей.
Подробнее об оксидативном повреждении клетки, антиоксидантной защите и системах репарации можно прочитать .
Митохондриальная теория
 Митохондриальная теория представляет собой частный случай свободнорадикальной теории. Митохондрия имеет свой аппарат репарации повреждений ДНК экзогенными и
Митохондриальная теория представляет собой частный случай свободнорадикальной теории. Митохондрия имеет свой аппарат репарации повреждений ДНК экзогенными и
эндогенными агентами, в роли которых чаще всего выступают , токсины, лекарства. Большое значение при повреждении мтДНК имеют близость к электрон- транспортной цеми и недостаток , защищающих ДНК. Оксидативное повреждение ДНК вызывает изменение оснований, появление AP-сайтов и другие виды повреждения. Наибольший вред наносит 8-оксогуанин, который накапливается в ДНК с возрастом . Повреждение мтДНК гораздо обширнее и сохраняется дольше, чем повреждение ядерной ДНК.
Многие исследования показали возраст- зависимый характер накопления повреждений мтДНК в скелетных мышцах (Lee et al., 1993), сердечной мышце (Marin-Garcia et al., 2002), мозге (Corral-Debrinski et al., 1992) и печени (Hamilton et al., 2001). Основную роль в повреждении играет 8-оксогуанин (de Souza-Pinto et al.,2001 , Hudson et al., 1998).
Уровень 8-оксогуанина в мтДНК (но не в ядерной ДНК) и максимальная
продолжительность жизни млекопитающих обратно пропорциональны.
Мутации в мтДНК игают огромную роль в повреждении таких постмитотичных клеток, как нейроны, и возникновении нейродегенеративных заболеваний. Митохондрии обеспечивают энергию, необходимую для функционирования синапсов, по которым передаются сигналы. Повреждение мтДНК в конечном итоге приводит к нарушению биоэнергетической составляющей нейрона.
Нейродегенеративные заболевания характеризуются прогрессирующей гибелью нейронов (). При нейродегенеративных заболеваниях были обнаружены мутации мтДНК и связанные с ними нарушения биоэнергетики (Kang and Hamasaki, 2005).
Более 50 лет назад было высказано предположение, что нарушения функционирования митохондрий имеют значение в канцерогенезе (Warburg, 1956). Было показано, что мутации в некоторых сайтах на мтДНК способствуют росту опухоли и снижению апоптоза (Shidara et al., 2005).
Из последних исследований на эту тему можно отметить работу Druzhyna NM, Wilson GL и LeDoux SP из Department of Cell Biology and Neuroscience , University of South Alabama , которые обобщили материал по связи митохондрий и старения за последние годы. Накопление повреждений ДНК в процессе оксидативного стресса- это основа свободнорадикальной теории старения Хармана (Harman, 2001) . Один из главных источников активных форм кислорода (АФК) в клетке- окислительное фосфорилирование в митохондриях. Повреждение мтДНК приводит к усилению синтеза АФК, что в свою очередь приводит к еще большему повреждению мтДНК- замыкается порочный круг, что в конце концов приводит к смерти клетки.
Сейчас проводится огромное количество исследований, связанных с митохондриями, окислительным стрессом и старением. Контраргументы для этой теории такие же, как и для свободнорадикальной (см. выше). Митохондриальную теорию выделяют отдельно из-за того, что митохондрия в клетке представляет собой "государство в государстве", т.е. работает автономно, имеет собственный геном и играет ключевую роль в явлении оксидативного стресса.
Теория гликозилирования белков
 Белки могут повреждаться сободными радикалами и через гликозилирование (Glycation, Maillard reaction, non-enzymatic glycosylation). Это реакция, в которой восстановленные сахара присоединяются к белку без участия ферментов (к амино-группам лизина и аргинина, которые вовлечены в построение пептидной связи).
Белки могут повреждаться сободными радикалами и через гликозилирование (Glycation, Maillard reaction, non-enzymatic glycosylation). Это реакция, в которой восстановленные сахара присоединяются к белку без участия ферментов (к амино-группам лизина и аргинина, которые вовлечены в построение пептидной связи). 
Amadori product-это кетоамин. Гликозилирование и образование Amadori product- обратимые реакции, окисление Amadori product с образованием AGEs- необратимая.
Тут теория гликозилирования белков переплетается со свободнорадикальной теорией: при образовании AGEs в клетке в 50 раз возрастает содержание свободных радикалов. Образование AGEs с поперечными сшивками в коллагене сосудов вовлечено в возникновение атеросклероза и нефропатии при диабете (Allen TJ et al., 1997), катаракты и болезни Альцгеймера.
Образование AGEs- универсальный признак старения в кожи, мышцах, легких, сосудах и др. органах.
Белки имет разную продолжительность жизни, кристаллины в хрусталике глаза существуют длительное время. Кристаллины хрусталика, коллаген и белки базальной мембраны чаще всего подвергаются поперечным сшивкам и формированию AGEs.
В экстрацеллюлярном матриксе стареющей кожи образуется продукт гликозилирования коллагена -глюкосепан (Sell et al, 2005).
Глюкосепан в 2 раза чаще встречается у диабетиков. При условии, что при диабете TGF−ß индуцирует образование внеклеточного матрикса, и этот матрикс постоянно гликозилируется, легко понять почему склеротические процессы усиливаются с возрастом.
Коллаген- самый часто встречающийся белок в организме млекопитающих. Поперечные сшивки в его стуктуре приводят к потере тканью эластичности, атеросклерозу, снижению функции почек, плохому заживлению ран, снижению жизненной емкости легких и катаракте.
Чаще всего в гликозилировании участвуют глюкоза, галактоза (в 5 раз более активна, чем глюкоза), фруктоза (в 8 раз), дезоксиглюкоза (в 25 раз), рибоза (в 100 раз) и дезоксирибоза (в 200 раз). Некоторые альдегиды, образующиеся при перекисном окислении липидов, гораздо активнее, чем сахара.
Сущетсвует специальное общество по изучении этой проблемы- International Maillard Reaction Society . Нынешний президент общества Дженифер Эймс (Jennifer M. Ames). Общество было основано в 2005 году и занимается исследованиями процессов гликозилирования в медицине, сельском хозяйстве и пищевой промышленности. В него входят ученые со всего мира, которые занимаются огранизацией конференций по проблеме активных углеводных соединений и просветительской работой. В Clinical Sciences Research Institute , University of Warwick проводятся исследования гликозилирования белков, его роли в повреждении клеток и старении. Недавно ученые из этого института- Найла Раббани (Naila Rabbani) и Пол Торнелли (Paul Thornalley) опубликовали статью- " Дикарбоновые сшивки повреждают электростанции: гликозилирование митохондриальных белков и оксидативный стресс" . Защита митохондриальных белков от гликозилирования эндогенными дикарбоновыми соединениями, метилглиоксалом и глиоксалом предотвращает увеличение продукции свободных радикалов и действие оксидативного стресса на протеом в течении жизни и в ходе старения у нематод. Это свидетельствует о том, что повреждение гликозилированием митохондриального протеома приводит к нарушению функционирования митохондрий, что в свою очередь приводит к оксидативному стрессу. В дальнейшем ученые надеются изучить белки, которые становятся мишенями для повреждения.
В Clinical Sciences Research Institute , University of Warwick проводятся исследования гликозилирования белков, его роли в повреждении клеток и старении. Недавно ученые из этого института- Найла Раббани (Naila Rabbani) и Пол Торнелли (Paul Thornalley) опубликовали статью- " Дикарбоновые сшивки повреждают электростанции: гликозилирование митохондриальных белков и оксидативный стресс" . Защита митохондриальных белков от гликозилирования эндогенными дикарбоновыми соединениями, метилглиоксалом и глиоксалом предотвращает увеличение продукции свободных радикалов и действие оксидативного стресса на протеом в течении жизни и в ходе старения у нематод. Это свидетельствует о том, что повреждение гликозилированием митохондриального протеома приводит к нарушению функционирования митохондрий, что в свою очередь приводит к оксидативному стрессу. В дальнейшем ученые надеются изучить белки, которые становятся мишенями для повреждения.
Теория гликозилирования белков является частным и самым распространенным случаем теории повреждения белков.
Поперечные сшивки нарушают строение белков и мешают им выполнять свои функции, отсюда нарушение функций клеток и органов. Эта теории согласуется со свободнорадикальной теорией. Однако имеет место парадокс "курицы и яйца"- что первично? Гликозилирование или оксидативный стресс? Гликозилирование приводит к оксидативному стрессу, при оксидативном стрессе увеличивается гликозилирование. На этот вопрос еще предстоит ответить, хотя большинство ученых склоняется к мысли, что первично гликозилирование.
Многое в этой теории остается непонятным:
1) Почему гликозилируются те или иные белки (помимо нахождения в составе аргинина и лизина)?
2) Есть ли порог повреждения, после которого клетка не может выполнять свои функции?
3) Как предотвратить патологическое гликозилирование?
4) Как регулируется гликозилирование?
Сейчас ведутся исследования по этим вопросам.
Повреждение ДНК и репарация
 В этом разделе можно отметить сразу несколько теорий- теория соматических мутаций (Szillard, 1959), теория накопления повреждений ДНК, теория генных мутаций. Все эти теории сводятся к тому, что старение развивается при нарушении генетических механизмов.
В этом разделе можно отметить сразу несколько теорий- теория соматических мутаций (Szillard, 1959), теория накопления повреждений ДНК, теория генных мутаций. Все эти теории сводятся к тому, что старение развивается при нарушении генетических механизмов.
Повреждение ДНК влияет на экспрессию генов, предотвращая транскрипцию ДНК в РНК или в результате появляется аномальный белок, который не может нормально функционировать. Многие мутации не являются летальными и сохраняются у делящихся клеток. Большинство исследователей склоняются к мысли, что повреждение ДНК важнее в процессе старения, чем мутации.
За 1 день в 1 клетке млекопитающего возникает около 200000 повреждений: окисление, гидролиз, алкилирование, повреждения ионизирующим излучением и химическими веществами. Удаление пурина или пиримидина (образование AP-сайта) чаще всего вызвано гидролизом или температурным воздействием:
Если AP-сайты не репарированы, то образуется однонитевой разрыв. также образуются и двунитевые разрывы. Также под действием ультрафиолета образуются тиминовые димеры (поперечные сшивки между соседними тиминами). Агенты, повреждающие ДНК, также повреждают и РНК и свободные нуклеотиды. Пурины и пиримидины в 100-1000 раз более чувствительны к модификации в виде мононуклеозидов и нуклеотидов, чем в составе ДНК и РНК, где они защищены спиральной структурой. Модификация пула нуклеотидов- это один из важных факторов повреждения нуклеиновых кислот. Хотя ДНК- и РНК- полимеразы распознают поврежденные и модифицированные основания, это распознавание недостаточно и они могут встроить поврежденные нуклеотиды в строящуюся нуклеиновую кислоту.
В этом теория повреждения ДНК сочетается со свободнорадикальной теорией.
В соответствии с вышеизложенным в 1963 Л. Оргелем (L.Orgel) была сформулирована теория ошибок
, которую он описал в статье "Поддержание правильного синтеза белка и связь с процессом старения ". Она основывается на предположении, что основной причиной старения является накопление с возрастом генетических повреждений в результате мутаций, которые могут быть как случайными (спонтанными), так и вызванными различными повреждающими факторами (ионизирующая радиация, стрессы, ультрафиолетовые лучи, вирусы, накопление в организме побочных продуктов химических реакций и другие)
. Гены, таким образом, могут просто терять способность правильно регулировать те или иные активности в связи с накоплением повреждений ДНК.
В то же время существует специальная система репарации, обеспечивающая относительную прочность структуры ДНК и надежность в системе передачи наследственной информации. В опытах на нескольких видах животных показана связь между активностью систем репарации ДНК и продолжительностью жизни. Предполагается ее возрастное ослабление при старении. Роль репарации отчетливо выступает во многих случаях преждевременного старения и резкого укорочения длительности жизни. Это относится, прежде всего, к наследственным болезням репарации (прогерии, синдром Тернера, некоторые формы болезни Дауна и другие). В то же время имеются новые данные о многочисленных репарациях ДНК, которые используются как аргумент против гипотез ошибок. В статье под названием «Наука отрицает старость» французский исследователь Р. Россьон (1995) полагает, что в свете этих фактов теория накопления ошибок в нуклеотидных последовательностях. требует пересмотра. Все же репарация, видимо, не приводит к 100% исправлению повреждений.
Теломеры
 В 1961 году американский геронтолог Л. Хейфлик установил, что человеческие фибробласты – клетки кожи, способные к делению, – «в пробирке» могут делиться не более 50 раз. В честь первооткрывателя это явление назвали «пределом Хейфлика». Однако Хейфлик не предложил никакого объяснения этому явлению.
В 1961 году американский геронтолог Л. Хейфлик установил, что человеческие фибробласты – клетки кожи, способные к делению, – «в пробирке» могут делиться не более 50 раз. В честь первооткрывателя это явление назвали «пределом Хейфлика». Однако Хейфлик не предложил никакого объяснения этому явлению.  В 1971 г. научный сотрудник Алексей Матвеевич Оловников, используя данные о принципах синтеза ДНК в клетках, предложил гипотезу, по которой «предел Хейфлика» объясняется тем, что при каждом клеточном делении хромосомы немного укорачиваются. У хромосом имеются особые концевые участки – теломеры, которые после каждого удвоения хромосом становятся немного короче, и в какой-то момент укорачиваются настолько, что клетка уже не может делиться. Тогда она постепенно теряет жизнеспособность – именно в этом, согласно теломерной теории, и состоит старение клеток. Открытие в 1985 г. фермента теломеразы, достраивающего укороченные теломеры в половых клетках и клетках опухолей, обеспечивая их бессмертие, стало блестящим подтверждением теории Оловникова. Правда, предел в 50-60 делений справедлив далеко не для всех клеток: раковые и стволовые клетки теоретически могут делиться бесконечно долго, в живом организме стволовые клетки могут делиться не десятки, а тысячи раз, но связь старения клеток с укорочением теломер является общепризнанной. Любопытно, что сам автор недавно решил, что теломерная гипотеза не объясняет причин старения, и выдвинул сначала еще одну, а потом и вторую, не менее фантастическую – луногравитационную . Обе они не получили ни экспериментального подтверждения, ни одобрения коллег.
В 1971 г. научный сотрудник Алексей Матвеевич Оловников, используя данные о принципах синтеза ДНК в клетках, предложил гипотезу, по которой «предел Хейфлика» объясняется тем, что при каждом клеточном делении хромосомы немного укорачиваются. У хромосом имеются особые концевые участки – теломеры, которые после каждого удвоения хромосом становятся немного короче, и в какой-то момент укорачиваются настолько, что клетка уже не может делиться. Тогда она постепенно теряет жизнеспособность – именно в этом, согласно теломерной теории, и состоит старение клеток. Открытие в 1985 г. фермента теломеразы, достраивающего укороченные теломеры в половых клетках и клетках опухолей, обеспечивая их бессмертие, стало блестящим подтверждением теории Оловникова. Правда, предел в 50-60 делений справедлив далеко не для всех клеток: раковые и стволовые клетки теоретически могут делиться бесконечно долго, в живом организме стволовые клетки могут делиться не десятки, а тысячи раз, но связь старения клеток с укорочением теломер является общепризнанной. Любопытно, что сам автор недавно решил, что теломерная гипотеза не объясняет причин старения, и выдвинул сначала еще одну, а потом и вторую, не менее фантастическую – луногравитационную . Обе они не получили ни экспериментального подтверждения, ни одобрения коллег.
Рассмотрим подробнее что такое теломера и как она укорачивается. Модель структуры теломер:
Схема двух конформаций теломеры. а
- "Т-петля". В этой конформации одноцепочечный G-хвост теломеры образует гетеродуплекс с ее двухцепочечным гомологичным районом. В результате образуется структура, получившая название Д-петли. б
- линейная конформация. Возможно существует непродолжительное время в процессе репликации ДНК. Предполагается, что в этой конформации теломераза имеет доступ к концу теломеры.
Основные белки, связывающиеся с теломерой:
Приведены только основные белки, которые участвуют в организации теломеры: Ku-гетеродимер. состоящий из субъединиц Ku70 и Ku80, белок Rap1, белки SIR2, SIR3 и SIR4, которые в комплексе взаимодействуют как с Rap1, так и с Ku-гетеродимером. Предполагается, что теломераза связывается с одноцепочечной концевой ДНК с помощью белка Estl.
У дрозофил есть механизм удлинения теломер, он до конца не ясен, но есть несколько моделей:
а
- Существующая модель предполагает удлинение теломер за счет транспозиции мобильных элементов. Снижение концентрации гипотетического белка А вызывает деблокирование белкового комплекса, который взаимодействует с белками, связанными с У концом LINE элемента. В результате происходит активизация транспозиций LINE-элементов. В нашей лаборатории было показано, что одним из белков, блокирующих присоединение элементов LINE, является гетерохроматиновый белок HP1 . б
-Альтернативная модель предполагает механизм генной конверсии/рекомбинации. При снижении концентрации гипотетического белка В происходит деблокирование свободного конца ДНК, что приводит к образованию гетеродуплекса с гомологичными теломерными последовательностями (аналог Д-петли в конформации "Т-петля" млекопитающих) и удлинению теломеры по механизму генной конверсии. В нашей лаборатории выделена мутация в гене, которая приводит к неконтролируемой генной конверсии по концу хромосомы.
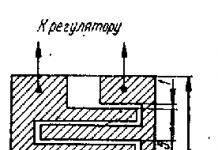
Элевационная теория Дильмана
 В начале 1950-х годов известный отечественный геронтолог В.М. Дильман выдвинул и обосновал идею о существовании единого регуляторного механизма, определяющего закономерности возрастных изменений различных гомеостатических (поддерживающих постоянство внутренней среды) систем организма. По гипотезе Дильмана, основным звеном механизмов как развития (лат. elevatio – подъем, в переносном смысле – развитие), так и последующего старения организма является гипоталамус – «дирижер» эндокринной системы. Главная причина старения – это возрастное снижение чувствительности гипоталамуса к регуляторным сигналам, поступающим от нервной системы и желез внутренней секреции
. На протяжении 1960-80-х гг. с помощью экспериментальных исследований и клинических наблюдений было установлено, что именно этот процесс приводит к возрастным изменениям функций репродуктивной системы и гипоталамо-гипофизарно-надпочечниковой системы, обеспечивающей необходимый уровень вырабатываемых корой надпочечников глюкокортикоидов – «гормонов стресса», суточные колебания их концентрации и повышение секреции при стрессе, и, в конечном итоге, к развитию состояния так называемого «гиперадаптоза». Следствием аналогичных возрастных изменений в системе метаболического гомеостата, регулирующего аппетит и энергетическое обеспечение функций организма, является нарастание с возрастом содержания жира в теле, снижение чувствительности тканей к инсулину (предиабет) и развитие атеросклероза.
В начале 1950-х годов известный отечественный геронтолог В.М. Дильман выдвинул и обосновал идею о существовании единого регуляторного механизма, определяющего закономерности возрастных изменений различных гомеостатических (поддерживающих постоянство внутренней среды) систем организма. По гипотезе Дильмана, основным звеном механизмов как развития (лат. elevatio – подъем, в переносном смысле – развитие), так и последующего старения организма является гипоталамус – «дирижер» эндокринной системы. Главная причина старения – это возрастное снижение чувствительности гипоталамуса к регуляторным сигналам, поступающим от нервной системы и желез внутренней секреции
. На протяжении 1960-80-х гг. с помощью экспериментальных исследований и клинических наблюдений было установлено, что именно этот процесс приводит к возрастным изменениям функций репродуктивной системы и гипоталамо-гипофизарно-надпочечниковой системы, обеспечивающей необходимый уровень вырабатываемых корой надпочечников глюкокортикоидов – «гормонов стресса», суточные колебания их концентрации и повышение секреции при стрессе, и, в конечном итоге, к развитию состояния так называемого «гиперадаптоза». Следствием аналогичных возрастных изменений в системе метаболического гомеостата, регулирующего аппетит и энергетическое обеспечение функций организма, является нарастание с возрастом содержания жира в теле, снижение чувствительности тканей к инсулину (предиабет) и развитие атеросклероза.
Эндокринная регуляция:
Важным этапом в развитии элевационной теории было установление роли возрастных изменений, закономерно возникающих в этих трех основных «супергомеостатах» (репродуктивном, адаптационном и метаболическом), в формировании таких имеющих ключевое значение для продолжительности жизни индивидуума феноменов, как метаболическая иммунодепрессия и канкрофилия, т.е. формирование условий, способствующих возникновению злокачественных новообразований. Развивая и углубляя на протяжении почти 40 лет свою концепцию, В.М. Дильман пришел к убеждению, что старение (и главные болезни, ассоциированные со старением) не
запрограммировано, а является побочным продуктом реализации
генетической программы развития и поэтому старение возникает с
закономерностью, свойственной генетической программе.
По концепции Дильмана, старение и связанные с ним болезни – это побочный продукт реализации генетической программы онтогенеза – развития организма.
Онтогенетическая модель возрастной патологии открыла новые подходы к профилактике преждевременного старения и болезней, связанных с
возрастом и являющихся основными причинами смерти человека: болезней сердца, злокачественных новообразований, инсультов, метаболической иммунодепрессии, атеросклероза, сахарного диабета пожилых и ожирения, психической депрессии, аутоиммунных и некоторых других заболеваний. Из онтогенетической модели следует, что развитие болезней и естественных старческих изменений можно затормозить, если стабилизировать состояние гомеостаза на уровне, достигаемом к окончанию развития организма. Если замедлить скорость старения
, то, как полагал В.М. Дильман, возможно увеличить видовые пределы жизни человека.
Современные представления о механизмах геропротекторного действия ограниченной по калорийности диеты, антидиабетических бигуанидов, пептидов эпифиза и мелатонина, некоторых нейротропных препаратов (в частности, L-ДОФА и ингибитора моноаминоксидазы депренила), янтарной кислоты свидетельствуют о перспективности такого подхода.
К сожалению, статей Дильмана в электронном виде пока нет, но можно прочитать его главный труд "Большие биологические часы" .
Таким образом, теория Дильмана является обобщением группы теорий программируемой гибели. Современный вариант теории Дильмана- нейроэндокринная теория . Одним из главных возраст-ассоциированных нарушений считается нечувствительность клеток к гормональным стимулам.
Иммунологическая теория
Известно, что с возрастом учащаются случаи различных инфекционных заболеваний, аутоиммунных процессов и опухолей. Возможно, это частично обусловлено возрастными дефектами иммунной системы. Связь столь широкого круга связанных с возрастом патологических процессов с дефектами иммунной системы привела к появлению предположения, что старение иммунной системы может ограничивать продолжительность жизни . Однако, несмотря на то, что выполнено множество экспериментальных и клинических исследований, свидетельствующих о возрастном истощении иммунной системы, имеющихся данных все же недостаточно для объяснения всех проявлений старения. Множество клеточных и гуморальных компонентов, вовлекаемых в иммунные реакции, и большое число модулирующих неиммунных факторов, которые также могут изменяться в старости, не позволяют и сегодня нарисовать исчерпывающую картину иммуностарения.
Иммунная и гемопоэтическая системы тесно связаны, поскольку имеют единое происхождение от общих полипотентных стволовых клеток. Обе играют ключевую роль в защите организма, предупреждении развития опухолей и возникновении ответа на инфекционные агенты. Однако оказывается, что с возрастом основной гемопоэз у животных и у человека или не изменяется, или изменяется минимально. Резервные возможности могут сужаться, что приводит к снижению способности реагировать на стрессорное воздействие.
Периферические лимфоидные органы, такие как селезенка и лимфатические узлы, с возрастом не претерпевают закономерных изменений в размерах. Возраст не вызывает каких-либо поражений костного мозга.
Продукция стволовых клеток, как правило, хорошо сохранена в старом
возрасте, хотя и имеются данные о слабых изменениях скорости их
деления. Считается, что инволюция тимуса, начинающаяся при половом созревании, является главным возрастным изменением иммунной системы. Такая инволюция состоит в прогрессивной потере клеточности с истощением лимфоидного пула клеток в зонах коры и кистозными изменениями эпителиальных клеток. Они являются источником различных пептидов, вовлекаемых в дифференцирующиеся лимфоидные клетки (Т-клетки) из более молодых лимфоидных клеток. Выход дифференцированных Т-клеток снижается с увеличением возраста. Прогрессивно снижаются синтез и секреция полипептидных гормонов тимуса, таких как тимозин, тимопоэтин и тимулин.
Считается установленным, что снижение эндокринной активности тимуса играет ключевую роль в возрастных дисфункциях иммунной системы, поскольку заместительная терапия введением гормонов способна восстановить различные иммунные функции в старости. Обмен цинка, который играет существенную роль в иммунокомпетенции. в старости снижается, тогда как добавки цинка могут восстановить иммунные функции.
Зрелые Т-клетки, В-клетки костного мозга и естественные клетки-киллеры (NК-клетки) могут быть определены в крови и лимфоидных органах с помощью специфических моноклональных антител.
У человека с помощью этого метода не выявлено существенных изменений соотношения различных субпопуляций лимфоцитов. Однако обнаружены серьезные изменения функционирования Т-лимфоцитов. В то время как общее количество Т-клеток в периферической крови в старости заметно не изменяется, наблюдаются четкие различия в относительном количестве подтипов Т-клеток. Количество незрелых лимфоцитов Т-предшественников увеличивается с возрастом, так же как и процент частично активированных Т-лимфоцитов, несущих маркеры незрелого фенотипа тимуса. Имеет место относительное увеличение цитотоксических супрессорных Т-клеток и уменьшение количества хелперов/индукторов Т-клеток. Функциональные дефекты клеточно-опосредованного иммунитета коррелируют с уменьшением популяции хелперов/индукторов. Клетки, полученные от старых людей или лабораторных животных, менее способны к ответу на аллогенные лимфоциты, фитогемагглютинин, конканавалин А и растворимый антиген. Лимфоциты от более старых мышей обладают меньшей
способностью вызывать реакции отторжения, чем те, которые получены от более молодых особей тех же инбредных линий. Половина здоровых людей в возрасте старше 50 лет страдают кожной гиперчувствительностью. Уменьшение количества хелперов/индукторов Т-клеток и функций клеточно-опосредованного иммунитета сопровождается ростом количества антител и аутоиммунных реакций.
Труднее выявить возрастные изменения гуморального иммунитета (функция В-клеток). Исследования влияния возраста на продукцию антител дают противоречивые результаты, возможно, из-за широкой вариабельности этих показателей, характерной для стареющих индивидуумов. Однако твердо установлено, что старение значимо ассоциируется с присутствием различных антител, особенно антител против ядерных антигенов. Получены также доказательства, что старение влияет на скорость продукции антител активированными В-клетками. Схема иммунного ответа в норме:
Что касается функциональных изменений, то их нарушения отмечены на различных уровнях. Во-первых, способность к пролиферации Т-клеток старых индивидуумов, как правило, снижена, вне зависимости от
стимуляции (антигенами, митогенами), и дефект касается как снижения
числа клеток, отвечающих на стимуляцию, так и преждевременного
истощения мощности клона отвечающих клеток. Подавляется ответ на многие интерлейкины, которые физиологически опосредуют модуляцию пролиферативной реакции. Этот феномен был зарегистрирован не только в отношении Т-клеток, но также и для NК-клеток, которые менее чувствительны в старом возрасте к действию интерлейкина-2 или интерферона. В отношении вспомогательных клеток (фагоцитов, макрофагов) известно, что их количество и функция не изменяются с возрастом, а при определенных обстоятельствах оказывается, что их активность усиливается.
Важным достижением в изучении механизмов иммуностарения стало установление роли в его развитии возрастных изменений в нервной и эндокринной системах. Связь между нервной и иммунной системами опосредуется гормонами и нейромедиаторами, которые достигают лимфоидных органов и клеток через кровь или прямые связи с вегетативной нервной системой. Нейроэндокринноиммунные
взаимодействия осуществляются циркуляцией гуморальных факторов
эпифизарно-гипоталамо-гипофизарной системы либо непосредственно
нейропептидами и гормонами либо опосредованно через действие
компонентов этой системы на секрецию гормонов периферических
эндокринных желез, которые также обладают иммуномодулирующей
активностью.
В экспериментах было продемонстрировано, что воздействие на старых
животных гормонами щитовидной железы, гормоном роста и аналогами
гормона, высвобождающего ЛГ, способно индуцировать реактивацию эндокринной функции тимуса восстанавливать различные связанные с возрастом периферические иммунодефициты, такие как функциональная полноценность Т-клеток, цитотоксичность NК-клеток.
По-видимому, нейроэндокринная система действует не только как модулятор иммунной системы, но также как мишень для сигналов, генерируемых в иммунной системе. Примерами подобных взаимодействий являются изменения нейроэндокринного баланса, которые могут быть индуцированы или удалением соответствующих лимфоидных органов (например, тимуса), или нарушением функции иммунной системы в результате реагирования на иммуногенные или толерогенные дозы антигена. Кроме того, зрелые лимфоидные клетки, стимулируемые антигеном, продуцируют гуморальные факторы, сходные (если не идентичные) с классическими гормонами и
нейромедиаторами (такими как АКТГ, ТТГ, гормон роста, пролактин,
гамма-адреналины). Эти реципрокные связи между нейроэндокринной и
иммунной системами имеют место в течение всей жизни, но приобретают особое значение в период старения.
Нейроэндокринная система:
В последние годы было установлено, что некоторые иммуномодуляторы,
в частности, пептидные препараты тимуса могут восстанавливать
компетентность иммунных клеток в старом организме и увеличивать
продолжительность жизни животных.
Механизмы старения достаточно сложны и многообразны. Сегодня существует несколько альтернативных теорий, которые отчасти противоречат друг другу, а отчасти – дополняют. Современная биология уделяет проблеме старения очень большое внимание, и с каждым годом появляются новые факты, позволяющие глубже понять механизмы этого процесса.
МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЕ ТЕОРИИ
Гипотеза, согласно которой причиной старения являются изменения генетического аппарата клетки, является одной из наиболее признанных в современной геронтологии.
Молекулярно-генетические теории подразделяются на две большие группы. Одни ученые рассматривают возрастные изменения генома как наследственно запрограммированные. Другие считают, что старение – результат накопления случайных мутаций. Отсюда следует, что процесс старения может являться или закономерным результатом роста и развития организма, или следствием накопления случайных ошибок в системе хранения и передачи генетической информации.
Теломерная теория
В 1961 году американский геронтолог Л. Хейфлик установил, что человеческие фибробласты – клетки кожи, способные к делению, – «в пробирке» могут делиться не более 50 раз. В честь первооткрывателя это явление назвали «пределом Хейфлика». Однако Хейфлик не предложил никакого объяснения этому явлению. В 1971 г. научный сотрудник Института биохимической физики РАН А.М. Оловников, используя данные о принципах синтеза ДНК в клетках, предложил гипотезу, по которой «предел Хейфлика» объясняется тем, что при каждом клеточном делении хромосомы немного укорачиваются. У хромосом имеются особые концевые участки – теломеры, которые после каждого удвоения хромосом становятся немного короче, и в какой-то момент укорачиваются настолько, что клетка уже не может делиться. Тогда она постепенно теряет жизнеспособность – именно в этом, согласно теломерной теории, и состоит старение клеток. Открытие в 1985 г. фермента теломеразы, достраивающего укороченные теломеры в половых клетках и клетках опухолей, обеспечивая их бессмертие, стало блестящим подтверждением теории Оловникова. Правда, предел в 50-60 делений справедлив далеко не для всех клеток: раковые и стволовые клетки теоретически могут делиться бесконечно долго, в живом организме стволовые клетки могут делиться не десятки, а тысячи раз, но связь старения клеток с укорочением теломер является общепризнанной. Любопытно, что сам автор недавно решил, что теломерная гипотеза не объясняет причин старения, и выдвинул сначала еще одну, редусомную, а потом и вторую, не менее фантастическую – луногравитационную. Обе они не получили ни экспериментального подтверждения, ни одобрения коллег.
Элевационная (онтогенетическая) теория старения
В начале 1950-х годов известный отечественный геронтолог В.М. Дильман выдвинул и обосновал идею о существовании единого регуляторного механизма, определяющего закономерности возрастных изменений различных гомеостатических (поддерживающих постоянство внутренней среды) систем организма. По гипотезе Дильмана, основным звеном механизмов как развития (лат. elevatio – подъем, в переносном смысле – развитие), так и последующего старения организма является гипоталамус – «дирижер» эндокринной системы. Главная причина старения – это возрастное снижение чувствительности гипоталамуса к регуляторным сигналам, поступающим от нервной системы и желез внутренней секреции. На протяжении 1960-80-х гг. с помощью экспериментальных исследований и клинических наблюдений было установлено, что именно этот процесс приводит к возрастным изменениям функций репродуктивной системы и гипоталамо-гипофизарно-надпочечниковой системы, обеспечивающей необходимый уровень вырабатываемых корой надпочечников глюкокортикоидов – «гормонов стресса», суточные колебания их концентрации и повышение секреции при стрессе, и, в конечном итоге, к развитию состояния так называемого «гиперадаптоза».
По концепции Дильмана, старение и связанные с ним болезни – это побочный продукт реализации генетической программы онтогенеза – развития организма. Онтогенетическая модель возрастной патологии открыла новые подходы к профилактике преждевременного старения и болезней, связанных с возрастом и являющихся основными причинами смерти человека: болезней сердца, злокачественных новообразований, инсультов, метаболической иммунодепрессии, атеросклероза, сахарного диабета пожилых и ожирения, психической депрессии, аутоиммунных и некоторых других заболеваний. Из онтогенетической модели следует, что развитие болезней и естественных старческих изменений можно затормозить, если стабилизировать состояние гомеостаза на уровне, достигаемом к окончанию развития организма. Если замедлить скорость старения, то, как полагал В.М. Дильман, можно увеличить видовые пределы жизни человека.
Адаптационно-регуляторная теория
Модель старения, разработанная выдающимся украинским физиологом и геронтологом В.В. Фролькисом в 1960-70-х гг., основана на широко распространенном представлении о том, что старость и смерть генетически запрограммированы. «Изюминка» теории Фролькиса состоит в том, что возрастное развитие и продолжительность жизни определяются балансом двух процессов: наряду с разрушительным процессом старения развертывается процесс «антистарения», для которого Фролькис предложил термин «витаукт» (лат. vita – жизнь, auctum – увеличивать). Этот процесс направлен на поддержание жизнеспособности организма, его адаптацию, увеличение продолжительности жизни. Представления об антистарении (витаукте) получили широкое распространение. Так, в 1995 г. в США состоялся первый международный конгресс по этой проблеме.
Существенным компонентом теории Фролькиса является разработанная им генорегуляторная гипотеза, по которой первичными механизмами старения являются нарушения в работе регуляторных генов, управляющих активностью структурных генов и, в результате, интенсивностью синтеза закодированных в них белков. Возрастные нарушения генной регуляции могут привести не только к изменению соотношения синтезируемых белков, но и к экспрессии ранее не работавших генов, появлению ранее не синтезировавшихся белков и, как результат, к старению и гибели клеток.
В.В.Фролькис полагал, что генорегуляторные механизмы старения являются основой развития распространенных видов возрастной патологии – атеросклероза, рака, диабета, болезней Паркинсона и Альцгеймера. В зависимости от активации или подавления функций тех или иных генов и будет развиваться тот или иной синдром старения, та или иная патология. На основе этих представлений была выдвинута идея генорегуляторной терапии, призванной предупреждать сдвиги, лежащие в основе развития возрастной патологии.
СТОХАСТИЧЕСКИЕ (ВЕРОЯТНОСТНЫЕ) ТЕОРИИ
Согласно этой группе теорий, старение – результат случайных процессов на молекулярном уровне. Об этом мы говорили выше: многие исследователи считают, что старение – это следствие накопления случайных мутаций в хромосомах в результате изнашивания механизмов репарации ДНК – исправления ошибок при ее копировании во время деления клеток.
Теория свободных радикалов
Практически одновременно выдвинутая Д.Харманом (1956) и Н.М.Эмануэлем (1958), свободнорадикальная теория объясняет не только механизм старения, но и широкий круг связанных с ним патологических процессов (сердечно-сосудистых заболеваний, ослабления иммунитета, нарушений функции мозга, катаракты, рака и некоторых других). Согласно этой теории, причиной нарушения функционирования клеток являются необходимые для многих биохимических процессов свободные радикалы – активные формы кислорода, синтезируемые главным образом в митохондриях – энергетических фабриках клеток.
Если очень агрессивный, химически активный свободный радикал случайно покидает то место, где он нужен, он может повредить и ДНК, и РНК, и белки, и липиды. Природа предусмотрела механизм защиты от избытка свободных радикалов: кроме супероксиддисмутазы и некоторых других синтезируемых в митохондриях и клетках ферментов, антиоксидантным действием обладают многие вещества, поступающие в организм с пищей – в т.ч. витамины А, С и Е. Регулярное потребление овощей и фруктов и даже несколько чашек чая или кофе в день обеспечат вам достаточную дозу полифенолов, также являющихся хорошими антиоксидантами. К сожалению, избыток антиоксидантов – например, при передозировке биологически активных добавок – не только не полезен, но может даже усилить окислительные процессы в клетках.
Старение – это ошибка
Гипотеза «старения по ошибке» была выдвинута в 1954 г. американским физиком М. Сциллардом. Исследуя эффекты воздействия радиации на живые организмы, он показал, что действие ионизирующего излучения существенно сокращает срок жизни людей и животных. Под воздействием радиации происходят многочисленные мутации в молекуле ДНК и инициируются некоторые симптомы старения, такие как седина или раковые опухоли. Из своих наблюдений Сцилард сделал вывод, что мутации являются непосредственной причиной старения живых организмов. Однако он не объяснил факта старения людей и животных, не подвергавшихся облучению.
Его последователь Л. Оргель считал, что мутации в генетическом аппарате клетки могут быть либо спонтанными, либо возникать в ответ на воздействие агрессивных факторов – ионизирующей радиации, ультрафиолета, воздействия вирусов и токсических (мутагенных) веществ и т.д. С течением времени система репарации ДНК изнашивается, в результате чего происходит старение организма.
Теория апоптоза (самоубийства клеток)
Академик В.П. Скулачев называет свою теорию теорией клеточного апоптоза. Апоптоз (греч. «листопад») – процесс запрограммированной гибели клетки. Как деревья избавляются от частей, чтобы сохранить целое, так и каждая отдельная клетка, пройдя свой жизненный цикл, должна отмереть и ее место должна занять новая. Если клетка заразится вирусом, или в ней произойдет мутация, ведущая к озлокачествлению, или просто истечет срок ее существования, то, чтобы не подвергать опасности весь организм, она должна умереть. В отличие от некроза – насильственной гибели клеток из-за травмы, ожога, отравления, недостатка кислорода в результате закупоривания кровеносных сосудов и т.д., при апоптозе клетка аккуратно саморазбирается на части, и соседние клетки используют ее фрагменты в качестве строительного материала.
Самоликвидации подвергаются и митохондрии – изучив этот процесс, Скулачев назвал его митоптозом. Митоптоз происходит, если в митохондриях образуется слишком много свободных радикалов. Когда количество погибших митохондрий слишком велико, продукты их распада отравляют клетку и приводят к ее апоптозу. Старение, с точки зрения Скулачева, – результат того, что в организме гибнет больше клеток, чем рождается, а отмирающие функциональные клетки заменяются соединительной тканью. Суть его работы – поиск методов противодействия разрушению клеточных структур свободными радикалами. По мнению ученого, старость – это болезнь, которую можно и нужно лечить, программу старения организма можно вывести из строя и тем самым выключить механизм, сокращающий нашу жизнь.
По мнению Скулачева, главная из активных форм кислорода, приводящих к гибели митохондрий и клеток – перекись водорода. В настоящее время под его руководством проходит испытания препарат SKQ, предназначенный для предотвращения признаков старения.
Основные научные теории и гипотезы старения человеческого организма
Лучшие врачи, философы, ученые всего мира в течение тысячелетий пытались найти и понять причины старения человеческого организма.
В настоящее время существует свыше двухсот различных научных теорий и гипотез старения. Однако ни одна из них не является общепризнанной. Почему все же человек стареет, достоверно неизвестно до сих пор. И теории пока остаются теориями.
Можно только надеяться, что современная наука вплотную уже приблизилась к разгадке этой тайны, способной изменить развитие будущей цивилизации.
В этой связи представляется весьма интересным проследить эволюцию взглядов ученых на причины старения организма, с древних времен и до наших дней.
1. Эволюция взглядов древних ученых на причины старения
Согласно древнегреческой медицинской концепции сущность жизни представлялась как равновесие между теплом, холодом, влажностью и сухостью.
Поэтому старение объяснялось потерей организмом внутреннего тепла и влаги, о чем еще в конце VI - начале V в. до н.э., писал древнегреческий философ Гераклит.
Другие древнегреческие ученые связывали процесс старения непосредственно с расходованием жизненной энергии и природного тепла.
В частности, один из величайших мыслителей всех времен и народов, блистательный философ Аристотель (384-322 гг. до н.э.) в своем трактате "О молодости и старости" писал: "Cтарение вызывается постепенным расходованием природного тепла, которое находится в каждом живом существе со дня его рождения. Центром этого тепла является сердце. Кровеносные сосуды разносят это тепло по телу и тем дают жизнь всем тканям и органам".
Выводы Аристотеля основывались на правильных наблюдениях, что выделение тепла в пожилом возрасте идет менее энергично, чем в молодости. С позиции наших современных знаний это следствие постепенного замедления обменных процессов.
Известный римский врач и естествоиспытатель, один из классиков античной медицины Гален Клавдий (129-201 н.э.) изучал процесс старения, используя именно такой подход.
Гален считал, что сущность жизни есть равновесие между элементарными физиологическими качествами: теплом, холодом, влажностью, сухостью.
С возрастом наступает изменение этих качеств у человека. Потеря тепла, влажности тканей, нарастание сухости составляют суть старости.
Гален ввел понятие дискразии как феномена старости, проявляющегося в потере теплоты и влажности тканей и нарастающей сухости человеческого тела. Тепло в те времена рассматривалось учеными как синонимом энергии, которая находилась в крови.
Позднее было доказано, что сухость кожи и потеря ее эластичности скорее не причина, а один из первых наиболее заметных внешних симптомов начала старения организма.
Древнегреческий врач, родоначальник атомистического учения, Асклепиад (около 128-56 гг. до н.э.), заслуги которого в медицине сравнивают с заслугами Гиппократа, считал, что человеческое тело состоит из мельчайших невидимых частиц, которые находятся в непрерывном движении. Их свободная циркуляция в организме и является главным условием здоровья.
Согласно его учению многие болезни и старение организма являются, прежде всего, следствием застоя этих частиц в сосудах тела.
Свой вклад в изучение причин старения внес величайший гений эпохи Возрождения, итальянский живописец, скульптор, архитектор, инженер и анатом Леонардо да Винчи (1452-1519), оставивший после себя огромное творческое наследие, среди которого видное место занимает фундаментальный труд: "Анатомия, записи и рисунки".
В этой фундаментальной монографии дается описание всех костей, внутренних органов, нервной и сосудистой систем, а также мышечного аппарата, сухожилий, хрящей и т.д. При этом описание сопровождается великолепными рисунками автора.
Здесь же Леонардо да Винчи приводит свое понимание причин старения организма и описывает этот процесс: "Старики, живущие в полном здравии, умирают от недостатка питания; и это происходит оттого, что у них беспрерывно сужается путь к венам брыжейки? вследствие утолщения оболочки этих вен вплоть до капиллярных вен, которые первыми закрываются совершенно.
Отсюда следует, что старики боятся холода больше, чем молодые, и что те, которые очень стары, имеют кожу цвета дерева или сухого каштана, потому что эта кожа почти лишена питания.
И с этой оболочкой вен у человека происходит то же, что в апельсинах, у которых кожа утолщается, а мякоть уменьшается по мере того, как они дряхлеют".
Некоторые ученые прошлого, в том числе немецкий зоолог профессор Мюнхенского университета Рихард Гертвиг (1850-1933), исходя из механистического понимания биологических закономерностей высказывали суждение, что к старости организм "срабатывается", подобно любой машине.
На самом деле ученые доказали, что в отличие от неживой природы все структуры живого тела не только постепенно разрушаются, но и непрерывно восстанавливаются. Механистическая теория старения оказалась не совсем верной.
Долгое время многие ученые и философы считали старость болезнью и тщетно в течение многих веков искали лекарство от этой болезни.
В своем трактате "О старости" Марк Туллий Цицерон (106-43 гг до н.э.) писал: "Как борются с болезнью, так надо бороться и со старостью: следить за своим здоровьем, есть и пить столько, сколько нужно для восстановления сил, а не для их угнетения".
4. Теория предельного деления клеток
Многие современные научные теории рассматривают процесс старения на клеточном уровне. В частности, одна из гипотез старения организма носит название "клеточной смерти" или теории предельного деления клеток.
Известно, что все системы и органы человека состоят из клеток. Всего в нашем организме, по оценкам ученых, насчитывается около 3 трлн клеток.
Наши клетки постоянно делятся, на смену старым приходят новые и т.д. Благодаря этому процессу в течение жизни организм имеет возможность обновляться и восстанавливаться.
За определенный отрезок жизни каждая мышца, каждый орган человека несколько раз "молодеет", как бы рождаясь заново. Однако с годами человеческий организм постепенно теряет эту драгоценную способность к обновлению.
Американский профессор анатомии медицинской школы Калифорнийского университета Леонард Хайфлик выдвинул гипотезу о том, что процесс старения связан с биологическим пределом способности клетки к делению.
В 1961 г., проводя серию экспериментов, ученый обнаружил определенные закономерности в процессах деления клеток.
Он предположил, что легочная ткань, по-видимому, отмирает после того, как ее клетки поделились определенное количество раз. Затем он экспериментально установил, что соматические (телесные) клетки могут делиться только ограниченное число раз.
Вероятно, в клетках существует своеобразный молекулярный счетчик. Он фиксирует, сколько делений уже сделано, и не дает клетке делиться сверх определенного генетически заданного предела.
Позднее, в 1969-1977 гг., проводя исследования человеческого эмбриона в Институте Уистара в Филадельфии, Хейфлик установил, что основная клеточная форма соединительной ткани организма, так называемые фибробласты клеток кожи делятся примерно 50 раз плюс-минус 10 раз, после чего процесс деления останавливается.
При этом у новорожденных клетки могут делиться 80-90 раз, а у стариков (70 лет и старше) только 20-30 раз.
Кроме того, в культуре ткани, т.е вне организма, клетки человека могут делиться также не больше 50 раз, после чего погибают.
Усложнив эксперимент, ученый взял клеточные культуры, которые были заморожены после того, как клетки разделились 25 раз. Оттаяв, эти клетки продолжили делиться, пока не достигли предела в 50 делений, а затем все же погибли.
Особо следует подчеркнуть, что когда клетки приближались к своему пределу деления, они начинали напоминать старую ткань с возрастными пигментами, которые обнаруживаются в постаревших клетках сердца и головного мозга.
Гибель клеток или ослабление функции в тех клетках, которые не подвержены делению, по окончании развития приводит к ослаблению организма.
В результате постепенно тело утрачивает способность к обновлению, а весь организм теряет возможность к восстановлению, что приводит к старению органов и систем.
Выявленные ученым закономерности получили название "порог Хайфлика".
Позднее было доказано, что в нашем организме существует два типа клеток - половые и стволовые, в которых присутствует теломераза, удлиняющая теломеры при помощи специальной РНК-матрицы.
Именно поэтому стволовые и половые клетки способны делиться бесконечно, копируя наш генетический материал для воспроизводства и выполняя функцию регенерации. Все остальные клетки человека не производят теломеразу и рано или поздно умирают.
Необходимо упомянуть еще об одном важном открытии британских ученых из университета Ноттингема. Внимание биологов давно привлекали плоские черви планарии, которые обладают экстраординарными способностями к регенерации.
Группа биологов изучила два вида этих червей, размножающихся половым путем и простым делением. Оба типа способны восстанавливать мышцы, кожу, внутренности и даже нервные окончания бесконечное количество раз.
Ученые пришли к выводу, что преимущество бесполых червей состоит в том, что во время регенерации количество теломеразы в их клетках резко возрастает. Наличие такого механизма потенциально может сделать их бессмертными.
Учёные из немецкого центра исследований раковых заболеваний (Deutsches Krebsforschungszentrum, DKFZ) в результате проведенных в 2011 г. исследований получили еще одно подтверждение, касающееся альтернативного механизма удлинения теломерных последовательностей с помощью ферментов, осуществляющих репарацию повреждений ДНК.
Ученые доказали, что клетки опухолей, в том числе раковые, научились обходить этот механизм и тем самым получили доступ к неограниченному количеству делений.
Это происходит при помощи активации уже упомянутой нами теломеразы - фермента, который в норме удлиняет теломеры эмбриональных клеток. Таким образом, опухолевые клетки "обнуляют" работу клеточных часов, что позволяет им делиться бесконечное количество раз.
Однако существует некоторое количество опухолей, примерно 10-15% от общего числа, клетки которых способны делиться бесконечно без активации теломеразы.
Клетки таких опухолей используют так называемый механизм альтернативного удлинения теломер (АУТ). Это связано с наличием в них ассоциированных ядерных телец (АЯТ).
На теломерах такие тельца формируются при участии PML-белков (promyelocytic leukemia). В нормальных клетках данные структуры не обнаруживаются.
Учёным из Мюнхенского университета, используя новую методику, удалось искусственно воссоздать в живых клетках ассоциированные ядерные тельца (АЯТ). Данную задачу удалось решить, присоединив к теломерам PML-белки и другие белки ассоциированных ядерных телец.
В ходе проведённых исследований учёные не только проанализировали сам процесс формирования телец, но и проследили за тем, что происходит впоследствии.
В частности, вновь сформированные ассоциированные ядерные тельца (АЯТ) индуцировали удлинение повторяющихся теломерных последовательностей. Удлинение происходило при помощи механизма репарации повреждений ДНК.
Полученные результаты впервые подтверждают тот факт, что ассоциированные ядерные тельца (АЯТ) играют важную роль в рамках альтернативного механизма удлинения теломер.
Можно предположить, что нарушение формирования ассоциированных ядерных телец (АЯТ) способно остановить пролиферацию положительных опухолевых клеток.
Результаты проведённых исследований, вероятно, можно будет использовать для борьбы с развитием опухолевых клеток. Однако функции ассоциированных ядерных телец (АЯТ) пока остаются до конца неизученными.
Многое в этой области еще предстоит выяснить. Тем не менее очевидно, что опыты с теломеразой открывают новые перспективы как в геронтологии, так и в онкологии для диагностики рака и, что особенно важно, для его лечения.
Следует упомянуть еще об одном результате эксперимента, проведенного учеными центра по изучению умственной деятельности и мозга Калифорнийского университета.
Целью эксперемента было выявление влияния занятий йогой и медитацией на процессы старения.
В частности, после трехмесячного курса медитации почти у всех участников эксперимента заметно повысился уровень фермента теломеразы, необходимого для построения теломер.
Таким образом, можно сделать вывод, что медитация может способствовать замедлению биологического процесса старения организма.
Видимо в состоянии транса в организме запускается определенная программа, способствующая росту выделения гормонов, в том числе ответственных за рост и репродуктивность.
Следует отметить, что существует гипотеза противоположная теории предельного деления клеток, согласно которой считается, что сама клетка бессмертна.
Дело просто в жидкой среде, в которой она находится и функционирует. Если найти механизм периодического обновления этой среды, то биение жизни может быть значительно продлено.
Найти такой механизм пытался известный французский хирург, биолог и патофизиолог Алексис Каррель (1873-1944), лауреат Нобелевской премии (1912).
Ученый и его коллеги взяли кусочек ткани сердца куриного эмбриона, и им удалось поддерживать клетки жизнеспособными и размножающимися при последующих переносах в свежую питательную среду.
Культивирование клеток привлекло всеобщий интерес, и линия клеток соединительной ткани поддерживалась в течение 24 лет, пережив самого ученого.
Таким образом, удалось увеличить продолжительность жизни птицы, как биологического вида фактически в 3,5 раза. В пересчете на жизнь человека это примерно 265-270 лет.
И еще один любопытный факт, подтверждающий гипотезу о возможном бессмертии живой клетки. В современных биомедицинских исследованиях и при разработке новых видов лечения часто используют выращенные в лаборатории культуры человеческих клеток.
Среди множества клеточных линий одной из самых известных является "HeLa" - клетки эндотелия матки. Эти клетки неприхотливы в культивировании, они очень хорошо переносят заморозку и консервацию.
На протяжении многих лет клетки были анонимными, ученые не знали, кому именно они принадлежали. Широкую известность клетки получили недавно и совершенно неожиданно.
Оказалось, что клетки были взяты у красивой чернокожей американки по имени Генриетта Лакс (Henrietta Lacks, 1920-1951). Она жила в небольшом городке Тернер в Южной Вирджинии вместе с мужем и пятью детьми.
В феврале 1951 г. она обратилась в госпиталь Джонса Хопкинса, где ей поставили диагноз рак шейки матки. Несмотря на хирургическую операцию и радиационное облучение, через восемь месяцев она скончалась. Было ей 31 год.
Пока Генриетта находилась в госпитале, ее лечащий врач отправил опухоль на анализ в лабораторию госпиталя. Оказалось, что клетки опухоли, обозначенные как "HeLa" (акроним имени и фамилии Henrietta Lacks), были уникальными, их можно было выращивать в искусственных условиях.
Размножались они вдвое быстрее клеток из нормальных тканей. Эти клетки пролиферируют необычайно быстро даже в сравнении с другими раковыми клетками.
В то время культивирование клеток вне организма было только на стадии становления, и главной проблемой была предопределённая гибель клеток. Как правило, после определенного количества делений вся клеточная линия погибала.
Трансформация сделала клетки "HeLa", фактически бессмертными - у них отключилась программа подавления роста после определенного количества делений, поэтому они способны делиться бесконечное число раз, в отличие от обычных клеток, имеющих предел Хайфлика.
Как позднее выяснилось, происходит это потому, что, как и все раковые клетки, клетки "HeLa" производят фермент теломеразу, которая наращивает теломеры на концах ДНК хромосом.
Руководитель лаборатории разослал штаммы клеток своим коллегам по всей стране. Вскоре спрос на клетки "HeLa" вырос, и их растиражировали в лабораториях по всему миру. Они стали первой "шаблонной" клеточной линией.
Эти клетки стали незаменимым инструментом для медицинских исследований. Миллиарды этих клеток покупались и продавались, при этом приносили значительные доходы.
Клетки "HeLa" заражали вирусом СПИДа, использовали для борьбы с полиомиелитом, отправляли в космос, скрещивали с клетками животных и растений, с их помощью раскрывали секреты раковых заболеваний, исследовали влияния ядерного взрыва на живые организмы, они помогли сделать важные шаги в изучении искусственного оплодотворения, клонирования и составления генетических карт.
Все это время семья Генриетты Лакс не подозревала об экспериментах с биологическим материалом их матери.
В начале этого века американская журналистка Ребекка Склут, бакалавр биологии и магистр изящных искусств в области творческой документалистики, преподаватель университета г. Мемфис, провела собственное расследование этого удивительного случая.
Период расследования начинается с 1950-х годов, когда Генриетта Лакс проходила лечение от рака, и продолжается до сегодняшних дней, когда дети и внуки Генриетты борются за наследственные права на биоматериал, взятый много лет назад у их матери без ее согласия.
В результате родилась книга "Бессмертная жизнь Генриетты Лакс", которая написана в жанре фэнтези и представляет собой фантасмагорию про сюрреалистические приключения человеческих клеток.
В 2010 г. книга в категории нон-фикшн стала бестселлером и побила все мыслимые рекорды продаж.
Генриетта Лакс была занесена в Книгу рекордов Гиннесса, как человек, чьи клетки через 60 лет после смерти все еще остаются живыми.
А как же предел деления клетки, о котором мы говорили выше? Вероятно, клетка действительно может делиться строго определенное количество раз, но если ученые смогут найти механизм обновления жизненной среды клетки и механизм удлинения теломер, то появится гипотетическая возможность увеличения количества их деления до бесконечности, как у опухолевых клеток или плоских червей планарий.
Еще одно доказательство связи процесса старения и развития раковых клеток нашли американские ученые. В 2012 г. исследователи из Онкологического центра Киммела в Джефферсоне выявили, что раковые клетки индуцируют окислительный стресс (аутофагию) в близлежащих клетках опухолевого микроокружения, в частности, в фибробластах, за счет чего питаются и растут.
Таки образом старение клетки и аутофагия метаболически поддерживают рост раковой опухоли и метастазирование.
Другими словами, нормальные, но стареющие соседние клетки занимаются приготовлением пищи для "кормления" рака. Старение в буквальном смысле обеспечивает раковую опухоль питанием.
Поскольку клеточное старение отражает биологическое старение, это исследование может объяснить, почему заболеваемость раком экспоненциально возрастает по мере старения организма.
Метастазирование может, в конечном счете, определяться старыми клетками в опухолевой микросреде, а не самими раковыми клетками.
Это открытие полностью может изменить взгляды на рак как на болезнь и ставит под сомнение устоявшееся мнение, что рак является клеточно-автономным генетическим заболеванием.
Напротив, из него следует, что рак, фактически, представляет собой болезнь старения организма-хозяина, подпитывающую рост опухоли и образование метастазов и определяющую, таким образом, клинический исход.
Поэтому нормально стареющие клетки организма-хозяина могут стать ключом к эффективной противораковой терапии.
Чтобы остановить рост опухоли и метастазирование, ученым необходимо "отключить подачу топлива", обеспечиваемую стареющими клетками, сделав мишенью аутофагию и старение клеток опухолевого микроокружения.
По мнению исследователей, это открытие означают смену парадигмы и вступление в совершенно новую эру разработки лекарственных средств для борьбы с раком.
Cвободно-радикальная теория
По своей сути к свободно-радикальной теории близка так называемая теория "перекрестных сшивок". Только роль агрессивных веществ здесь играют сахара, в первую очередь всегда присутствующая в организме человека глюкоза.
Сахара могут вступать в химическую реакцию с различными белками. При этом функции этих белков могут нарушаться. Потенциальная опасность такой реакции заключается в том, что молекулы сахаров, соединяясь с белками, обладают способностью "сшивать" молекулы белков между собой. В результате клетки начинают хуже работать. В них накапливается клеточный мусор.
Как полагают ученые, одним из проявлений такой сшивки белков является потеря тканями эластичности. Визуально это проявляется в виде морщин на коже. Но более значительный вред организму приносит потеря эластичности кровеносных сосудов и лёгких.
В принципе у клеток есть механизмы для разрушения подобных сшивок. Но этот процесс, по мнению ученых, требует от организма очень больших энергетических затрат.
В настоящее время разработаны лекарственные препараты, которые разбивают внутренние сшивки и превращают их в питательные вещества для клетки.
Теория апоптоза
Термин "апоптоз", что в переводе с греческого означает "опадание листьев", ввел в научный оборот еще древнеримский врач Гален.
Он заметил, что если надломить ветку, с которой уже начала опадать листва, то листопад прекращается и листья, хотя и меняют цвет, засыхают, но все же остаются на ветке.
То есть опадание листьев, в отличие от их омертвления на сломанной ветке, - физиологический процесс, преднамеренное самоубийство листьев.
В современной науке термин "апоптоз" применяется к физиологическому явлению - самоубийству клеток.
Впервые мысль о том, что процесс старения как завершающий этап индивидуального развития организма может быть запрограммирован, высказал немецкий зоолог и теоретик эволюционного учения Август Вейсман (1834-1914).
Один из крупнейших современных биохимиков, наш соотечественник академик Владимир Петрович Скулачев (1935 г. рождения), развивая научные идеи Августа Вейсмана о запрограммированной смерти, выдвинул свою гипотезу старения.
Ученый считает, что старение - это не столько накопление поломок в организме, ведущих к смерти, сколько запускаемая на генном уровне программа апоптоза.
По мнению академика, клетки "уходят в апоптоз" по многим причинам. Одна из основных - появление "бездомных" клеток. Клетки в организме "привязаны" к определенному органу и существуют только в соответствующем биохимическом окружении.
И если вдруг какая-либо клетка случайно попадает в "чужой" орган или ткань, то она быстро "кончает жизнь самоубийством".
Или другой пример - развитие человеческого эмбриона. На определенной стадии у него появляется хвост, который потом исчезает. Клетки хвоста тоже "уходят в апоптоз".
Предраковые клетки также уничтожают сами себя с помощью апоптоза. Ученые считают, что в половине случаев рак появляется тогда, когда "ломается" ген, кодирующий белок p 53, который "следит" за изменениями и мутациями в ДНК.
При их обнаружении он посылает предраковой клетке с измененным генетическим материалом сигнал "покончить жизнь самоубийством".
Клетка самоубийца отмирает безболезненно, она как бы сама себя разбирает на части, которые соседние клетки впоследствии используют в качестве строительного материала.
Этим апоптоз отличается от травматической гибели клеток - некроза, когда разрывается клеточная мембрана и содержимое клетки вытекает наружу.
По мнению академика В. Скулачева, апоптоз необходим организму еще и для "дезинфекции". Клетка, зараженная вирусом, получает биохимический сигнал на самоуничтожение.
Ученый называет это явление "самурайским законом биологии" - лучше умереть, чем ошибиться. На научном языке суть этого закона заключается в том, что во всех живых системах, начиная с внутриклеточных органелл до человеческого организма, существует система самоликвидации клеток. С помощью апоптоза природа выбраковывает плохие и лишние клетки,
Другие теории старения
Нарушения высшей нервной деятельности и функций головного мозга
Выдающийся русский физиолог, лауреат Нобелевской премии, академик И.П. Павлов (1849-1936) и его последователи считали причиной старости функциональные нарушения высшей нервной деятельности.
Гипотезу о ведущей роли нервной системы в генезисе старения развивали его ученики - академики Алексей Сперанский и Иван Сеченов.
Французские ученые предлагают считать причиной и началом старения снижение когнитивных функций головного мозга человека.
Известно, что в большинстве случаев развитие старческого слабоумия фиксируется к 60 годам. Однако процессы, ведущие к проявлению этого возрастного недуга, начинаются уже в 40-45 лет и ранее. Именно в этом возрасте клетки мозга начинают постепенно и неминуемо отмирать, а познавательные функции мозга и память начинают заметно ухудшаться.
В США в 1973 г. в научных трудах Чикагского университета была опубликована работа, в которой доказывалось, что основной причиной старения людей является постепенное оседание шлаков в межклеточных пространствах, в том числе и в клетках коры головного мозга.
Снижение гормонального фона и регрессия половых желез организма
Важная роль в организме человека принадлежит гормонам, биологически высокоактивным веществам, оказывающим регулирующее влияние на функционирование органов и систем организма.
В частности, гормон роста действует синергично с половыми гормонами, обеспечивая нашу сексуальную активность, оказывая влияние на процессы регенерации, сохранения здоровья, как физического, так и умственного.
Именно половые гормоны отвечают в нашем организме за внешнюю привлекательность, мужественность фигуры и внешности у мужчин и женственность фигуры и привлекательность у женщин.
От уровня половых гормонов зависит и наша сексуальная активность. Однако, как считают ученые, после 30 лет у человека начинается уменьшение выработки гормонов примерно на 1-3% в год, к 50 годам общее падение достигает 30%.
Поэтому австрийский ученый, хирург Эйген Штейнах (1861-1944) видел одну из причин старения в регрессии половых желез организма.
В качестве средства омоложения предлагал стимулирующее действие на мужскую железу путем перевязки семявыводящего протока и ксенотрансплантацию, т.е. под?садку кусочка донорского семенника. В качестве донора может выступать человек или обезьяна. Об этом методе омоложения мы более подробно расскажем в следующих разделах монографии.
Элевационная теория старения
В начале 50-х годов прошлого века ленинградским ученым Владимиром Дильманом была выдвинута и обоснована так называемая элевационная теория старения, которая также связана с нарушениями гормонального фона.
Согласно этой теории механизм старения начинает свою работу с постоянного возрастания порога чувствительности гипоталамуса к уровню гормонов в крови.
Гипоталамус - это часть головного мозга, которой принадлежит основная роль в поддержании уровня обмена веществ, в регуляции деятельности пищеварительной, сердечно-сосудистой, эндокринной и других физиологических систем.
При повреждениях гипоталамуса возникают эндокринные, обменно-трофические или вегетативные нарушения, в том числе сдвиги терморегуляции, сна и бодрствования, эмоциональной сферы.
В итоге увеличивается концентрация циркулирующих в крови гормонов. В результате возникают различные формы патологических изменений в организме, характерные для старческого возраста
Это приводит к таким специфическим заболеваниям, как ожирение, диабет, атеросклероз, канкриофилия, депрессия, метаболическая имуннодепрессия, гипертония, гиперадаптоз, автоиммунные заболевания, климакс и др. Эти болезни ведут к преждевременному старению и в конечном итоге к смерти.
Снижение числа стволовых клеток
Одна из теорий старения связана со стволовыми клетками. Как показывают научные исследования, с возрастом количество стволовых клеток в организме катастрофически снижается.
Если у новорожденного человека одна стволовая клетка приходится на 10 тыс. обычных, то к 50 годам одна стволовая клетка приходится уже на 500 тыс. обычных клеток организма.
Истощение запаса стволовых клеток лишает организм возможностей самовосстановления, и как следствие начинают доминировать процессы старения организма.
Снижение способности коллоидных веществ связывать воду
Многие ученые считают одной из причин старения организма снижение способности коллоидных веществ, особенно белков, связывать большое количество воды.
Вода является основной средой, в которой протекают многочисленные химические реакции и физико-химические процессы, лежащие в основе жизни.
Человеческий организм строго регулирует содержание воды в каждом органе и каждой ткани. Постоянство внутренней среды организма, в том числе и определённое содержание воды, - одно из главных условий нормальной жизнедеятельности.
По мере старения человека количество воды в теле снижается. Так, например, в теле 3-х месячного плода 95% воды, у новорождённого ребенка уже 70%, у взрослого человека около 55-65%.
В организме взрослого человека с массой тела 65 кг содержится в среднем 40 литров воды, из них около 25 литров находится внутри клеток и 15 литров - в составе внеклеточных жидкостей организма.
Изменение генетического аппарата клетки
Согласно молекулярно-генетической гипотезе В.В. Фролькиса (1924-1999) - современного физиолога и геронтолога, вице-президента АМН Украины к числу первичных причин старения можно отнести изменение генетического аппарата клетки.
Наиболее обоснованной считается теория соматических мутаций. В соматических клетках (клетках тела) могут спонтанно проходить мутации, которые отрицательно влияют на ее функционирование. Накопление таких мутаций ведет к нарушению функций организма, к старению и в конце концов к смерти.
Известный английский генетик Обри ди Грей из Кембриджского университета на протяжении многих лет изучает митохондрии - энергетические фабрики клеток. По его мнению, старение организма обусловлено молекулярными и клеточными повреждениями. Прежде всего это относится к митохондриям, как только они выходят из строя, человек начинает стареть.
Сокращение массы мышц
Известный советский хирург, академик Н.М. Амосов (1913-2002) также считал, что старение запрограммировано в генах, все другие факторы, влияющие на этот процесс второстепенны.
Проявление старости выражается в сокращении массы мышц. Это ведет к уменьшению физической силы и переносимости нагрузок, что ещё больше ограничивает дееспособность. Он писал: "Получается так: старость - это меньше движений, меньше мышц, меньше силы, и следствие всего этого - новое ускорение старения".
Снижение активности ферментов
Современные российские учёные, в частности В.В. Алпатов и О.К. Настюкова считают, что старение организма является следствием снижения активности ферментов.
Таким образом, проведенный анализ основных теорий и гипотез старения организма позволяет сделать основной вывод, что старение, вероятнее всего, происходит на клеточном уровне.
При этом многие отечественные и зарубежные геронтологи приходят к консенсусу, рассматривая старение как генетически запрограммированную органическую смерть организма. Этот процесс биологи назвали феноптозом.
На уровне конкретного человеческого организма процесс старения можно также представить как нарастание энтропии, снижения и, наконец, коллапса его энергетического и информационного обмена.
Хотелось бы обратить внимание на одно явное противоречие биологической природы человека. С рождения в организме заложена мощнейшая иммунная система защиты человека от внешних неблагоприятных факторов, различных болезней и преждевременной смерти.
С этой точки зрения процесс запрограммированного старения и смерти выглядит совершенно противоестественным и бессмысленным для человеческого организма, который до самой смерти продолжает бороться с болезнями.
Можно предположить, что это две не пересекающиеся между собой отдельные генетические, информационные программы, функционирующие на разных уровнях организма.
Вместе с тем в настоящее время среди ученых все большую популярность приобретает эпигенетическая теория старения, которая утверждает, что оно не запрограммировано в геноме человека, а происходит из-за постоянного повреждения ДНК, приводящего в итоге к гибели организма.
Признаки старения проявляются на разных уровнях организации ор-
ганизма: молекулярном, клеточном, тканевом, системном, организменном.
На организменном уровне - внешние признаки: изменение осанки,
формы тела, уменьшение размеров тела, седина, потеря эластичности ко-
жи, морщины, ослабление зрения слуха, ухудшение памяти, истончение
компактного и губчатого вещества кости, изменение лицевого отдела че-
репа. Уменьшается жизненная сила легких, увеличивается артериальное
давление, атеросклероз, ослабление функций щитовидной железы, умень-
шение функций половых гормонов, уменьшение основного обмена.
На клеточном уровне - уменьшение воды в цитоплазме, изменение
активного транспорта ионов, усиление гликолиза, снижение содержания
АТФ, креатинфосфата в сердце, мозге, скелетных мышцах, изменяется
РНК и ДНК.
На молекулярном - возникают ошибки считывания информации с
РНК и нарушение синтеза определенных белков. В цитоплазме клетки на-
капливаются свободные радикалы. Ассимиляция не восполняет диссими-
ляцию. Снижается митотическая активность, усиливаются хромосомные
абберации. Однако многие гомеостатические показатели не изменяются:
артериальное давление, частота сердечных сокращений, ЭКГ, ЭЭГ, уро-
вень сахара в крови, анализ желудочного сока.
Возрастные изменения бывают разными: показатели одних снижаются
(сокращения сердца, функция щитовидной железы, острота зрения); а других -
не меняются (сахар в крови, эритроциты, лейкоциты, гемоглобин); у третьих -
повышаются (синтез гипофизарных гормонов, уровень холестерина в крови,
чувствительность клеток к гуморальным и химическим факторам).
Возрастные изменения проявляются в разные периоды. Так, атрофия
тимуса возникает у человека в 13–15 лет, угасание функций яичников - в
48–52 года. В костной ткани изменения возникают рано, но развиваются
медленно, в ЦНС - поздно, но быстро.
Получается парадокс, над которым задумывался еще Демокрит. Он
писал: «Старость - есть повреждение всего тела при полной неповреж-
денности всех его частей». Это кажущееся противоречие имеет глубокий
биологический смысл. Несмотря на структурные изменения при старении,
благодаря процессам регулирования возникают приспособительные механиз-
мы. Они противодействуют угасанию обмена и функций, содействуют их со-
хранению или противостоят резкому изменению. Вот почему на определенном
этапе старения, несмотря на некоторые очевидные структурные изменения,
может сохранится еще оптимальный уровень деятельности ряда систем.
Старение - это неизбежно и закономерно нарастающий во времени,
развивающийся задолго до старости многозвеньевой процесс, неизбежно
ведущий к сокращению приспособительных возможностей организма, уве-
личению вероятности смерти. Старение - результат ограничения меха-
низмов саморегуляции, снижения их потенциальных возможностей при
первичных изменениях в регулировании генетического аппарата.
Для объяснения процессов старения к настоящему времени выдвинуто
около 300 различных гипотез, большинство из которых представляют только
исторический интерес: энергетическая (М. Рубнер), гормональная (С. Воро-
нов), интоксикационная (И. Мечников), перенапряжение ЦНС (И. Павлов),
соединительнотканная (А. Богомолец), адаптационно-регуляторная (В. Фрольк-
сис) и генетическая или программная. Единой теории нет.
Геронтология сегодняшнего дня стремится раскрыть первичные изме-
нения и все последующие цепи причинно-следственных связей, ведущих к
глубоким нарушениям деятельности организма. Большинство исследова-
телей согласны с тем, что первичные механизмы старения связаны с нару-
шениями в генетическом аппарате, в биосинтезе белков.
Предпосылками этих взглядов являются следующие факты. Продол-
жительность жизни - видовой признак. Следовательно, механизмы, опре-
деляющие продолжительность жизни, каким-то образом закреплены в ходе
эволюции, предопределены в онтогенезе организма.
Если учесть, что существует определенная последовательность функ-
ций генов-регуляторов (одни из них изменяются раньше и значительно,
другие - практически не изменяются, третьи - активируются), то станет
понятной неравномерность, разнонаправленость проявления процессов
старения организма.
В 1975 г. В. В. Фрольксис выступил с обоснованием адаптационно-
регуляторной теории старения, согласно которой старение сложный мно-
гокомпонентный внутренне противоречивый процесс нарушения жизне-
деятельности организма, и процесс возникновения важных мобилизацион-
ных приспособительных механизмов, процесс угасания обмена и функции
и возникновение активных механизмов их подавления. Первичные изме-
нения при старении развиваются в регуляторных генах, которые приводят
к нарушению деятельности клетки, ее гибели.
Изучалась связь между старением организма и числом делений его
соматических клеток. Выявлено, что число делений клеток уменьшается с
увеличением возраста донора.
Благодаря механизмам саморегуляции в ходе старения возникают
важные приспособительные механизмы на разных уровнях жизнедеятель-
ности организма (усиление чувствительности к медиаторам и гормонам).
Они во многом определяют продолжительность жизни особи. Значение их
не абсолютное. В ряде случаев, сопровождающие адаптационные меха-
низмы сдвиги могут способствовать нарушению метаболизма организма.
Смерть - закономерное явление. Она подготавливается всем ходом
онтогенеза. Смерть всегда находит свое выражение в форме той или иной
случайности. Смерть человека даже в глубокой старости наступает в ре-
зультате разных причин (при нарушении согласованности обменных про-
цессов в организме, и организма со средой). Случайные причины могут
вызвать преждевременную смерть в любом периоде онтогенеза.
Биология доказала, что смерть - это медленный, последовательно со-
вершающийся процесс. После смерти организма как целого, его части про-
должают некоторое время жить и погибают в известной последовательности
(клетка коры мозга →клетки печени →сердце →перефирические органы).
Современная наука позволила уточнить понятие «смерть». Советский
ученый В. А. Неговский предложил различить клиническую и биологиче-
скую смерть. Клиническая смерть характеризуется прекращением сокраще-
ний сердца, отсутствием дыхания, рефлекторных реакций. Однако – это пер-
вый и еще обратимый процесс умирания. В момент клинической смерти все
органы и ткани остаются живыми, их метаболизм остается упорядоченным.
Ее продолжительность 3–5 минут. В состоянии клинической смерти можно
добиться восстановления жизнедеятельности организма. В настоящее время
методы оживления организма человека успешно используются в клинике.
Биологическая смерть наступает позже и характеризуется неупорядо-
ченными химическими реакциями в клетках, автолизом и разложением
ткани. Биологическая смерть - процесс необратимый.
Процесс старения и причины старения волновали и будут волновать умы пока еще смертных и подверженных болезням людей. Поисками бессмертия человечество занимается на протяжении многих веков, пытаясь раскрыть тайные причины старения, обуздать процесс старения и строя заманчивые, но пока еще не совершенные теории старения.
Идеи и труды ученых античного мира, алхимиков из средневековья, философов и естествоиспытателей дожили до наших дней, намного пережив своих создателей.
Несмотря на неудачи, поиски бессмертия не прекратились и сейчас, но теперь за них основательно взялись ученые, имеющие в своих руках новейшие технологии и самые современные знания.
Наука геронтология, возникшая около полувека назад, приняла эстафетную палочку в борьбе со смертью и попытках обмануть процессы старения человеческого организма.
Но для того, чтобы бороться со старостью, для начала необходимо разобраться в ее природе. Но, до сих пор, единого и очевидного взгляда на механизмы и причины старения не существует.
Теория засорения Мечникова
В настоящее время существует несколько десятков теорий старения. Одной из первых теорий – была теория русского биолога Ильи Мечникова, который предположил, что главной причиной старения является засорение организма ядами, образовавшимися в кишечнике. Способы отложить преждевременное старение, основанные на этих взглядах основательно прижились в современной практике сохранения здоровья в виде очистительных клизм, разгрузочных дней, диет, выводящих шлаки и т.д.
И не смотря на то, что теория Мечникова подверглась обоснованной критике, некоторые методы, изначально базирующиеся на ней, действительно работают. Например, те люди, которые питаются умеренно, живут дольше и реже болеют.
Правда это явление в настоящее время имеется и другой взгляд, основанный на идее единства процессов роста и старения, которые запускаются и контролируется так называемым белком TOR. Белок TOR необходим для развития и роста молодого организма, однако, по окончании процесса развития, он становится причиной старения и появления возрастных заболеваний. Внешние действия, замедляющие рост, одновременно замедляют и процессы старения, тем самым увеличивая продолжительность жизни. Например, низкокалорийная диета замедляет рост, но увеличивает продолжительность жизни. В настоящее время изучаются способы подавления активности белка TOR с помощью фармакологических препаратов, а один из таких препаратов (рапамицин) даже применятся в трансплантологии в борьбе с процессами отторжения органов.
Свободно-радикальная теория старения
Наиболее распространенной теорией старения на сегодняшний день является свободно-радикальная теория. Автором, выдвинувшим ее в 1956 году, является Денхан Харман. Он предположил, что механизмы старения обусловлены окислением биополимеров активными формами кислорода. Образование так называемых свободных радикалов постоянно происходят внутри наших клеток (в митохондриях) в процессе жизнедеятельности, а также усиливается при действии токсинов (например при курении или употреблении алкоголя) и радиации. Свободные радикалы – это молекулы, потерявшие один электрон и поэтому ставшие необычайно активными. Для того чтобы вернуть себе устойчивость они отбирают электроны у здоровых молекул, тем самым повреждая их. Под действием свободных радикалов происходит повреждение различных клеточных структур, например клеточных мембран, нуклеиновых кислот, белков и липидов. Повреждение клетки и макромолекул в результате действия активных форм кислорода называется оксидативным стрессом.
Когда свободных радикалов становится слишком много, клетки не успевают нейтрализовать их и восстанавливать свои поврежденные структуры и либо гибнут, либо перерождаются, запуская механизмы роста раковых опухолей и процесс старения.
Роль свободных радикалов в развитии таких заболеваний как болезнь Альцгеймера, катаракта, атеросклероз, дегенеративные заболевания суставов и позвоночника, некоторых видов злокачественных опухолей считается доказанной.
Как и в случае с теорией старения Мечникова, на основе свободно-радикальной теории возникло множество популярных способов сохранить здоровье и предотвратить преждевременное старение. В основе их лежит борьба с процессами окисления и образованием свободных радикалов. По мнению многих специалистов, профилактика старения с точки зрения свободно-радикальной теории заключается в здоровом образе жизни, отказе от алкоголя и курения, в занятиях спортом и здоровом питании, своевременном приёме витаминов и антиоксидантов.
В то же время действие антиоксидантов, входящих в множество БАДов некоторыми учеными ставится под сомнение. Дело в том, что, по их мнению, они действуют на весь организм без разбора и вовсе не там где от них требуется. В результате они разрушают защитные силы организма и нередко вредят. Кроме того, природные легко распознаются организмом и быстро выводятся.
И, тем не менее, идея антиоксидантов продолжает свое развитие.Российский академик Скулачев уже на протяжении нескольких лет проводит разработку и испытания революционного антиоксиданта, который действует избирательно и приостанавливает процесс старения организма.
Эксперименты, проводимые Скулачевым на подопытных животных дают положительные результаты. Подопытные животные живут вдвое дольше, не знают инфарктов, инсультов, гипертонии. Они не заболевают катарактой, глаукомой и дистрофией сетчатки.
Однако полностью остановить запрограммированную смерть академику Скулачеву пока не удалось. Прожив долгую жизнь, подопытные животные заболевают раком и умирают. В связи с этим, Скулачев считает, что рак – это тоже программа, предусмотренная природой в качестве механизма самоуничтожения.
И действительно, если живые организмы перестанут умирать, а поколения сменять друг друга, то остановятся процессы эволюции, а значит, не будет происходить и совершенствование человека. Об эволюционной теории старения и других теориях будет рассказано в следующих статьях, а пока можно подвести некоторые итоги.
На основании описанных теорий старения, можно сделать вывод: для того чтобы продлить свою жизнь и сохранить здоровье необходимо выполнять следующее:
- Вести активный образ жизни.
- Правильно и умеренно питаться.
- Избавиться от вредных привычек.
- Избегать контакта с вредными веществами и радиацией на производстве и в быту.
- Принимать и антиоксиданты.
Одним словом, для того, чтобы замедлить процесс старения, необходимо вести здоровый образ жизни.
Видео процесс старения за 40 секунд:
Видео о здоровом образе жизни, здоровом питании и замедлении старения: