Глава 3.
Вещества, действующие на холинергические синапсы (фармакология)
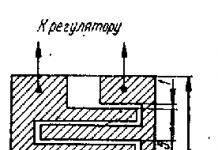
На рисунке 10 показана схема синапса, в котором возбуждение передается с помощью ацетилхолина. Ацетилхолин синтезируется в цитоплазме холинергических нервных окончаний из ацетилкоэн-зима А и холина; путем активного транспорта проникает в везикулы и депонируется в везикулах.
При поступлении нервных импульсов происходит деполяризация мембраны нервного окончания, открываются потенциал-зависимые кальциевые каналы, ионы Са 2+ поступают в цитоплазму нервного окончания и способствуют взаимодействию белков мембраны везикул с белками пресинаптической мембраны. В результате везикулы встраиваются в пресинаптическую мембрану, открываются в сторону синаптической щели и высвобождают ацетилхолин.
Рис. 10. Холинергический синапс.
ХАТ - холинацетилтрансфераза; АцКоА - ацетилкоэнзим А; Ацх - ацетилхолин;
АХЭ - ацетилхолинэстераза.
Ацетилхолин возбуждает рецепторы постсинаптической мембраны (холинорецепторы) и расщепляется ферментом ацетилхолин-эстеразой на холин и уксусную кислоту. Холин подвергается обратному захвату нервными окончаниями (обратный нейрональный захват) и вновь участвует в синтезе ацетилхолина.
Известны вещества, действующие на разные этапы холинергической передачи.
Везамикол блокирует вход ацетилхолина в везикулы.
Ионы Mg 2+ и аминогликозиды препятствуют входу Са 2+ в нервное окончание через потенциал-зависимые кальциевые каналы (аминогликозиды могут нарушать нервно-мышечную передачу).
Ботулиновый токсин вызывает протеолиз синаптобревина (белок мембраны везикул, который взаимодействует с белками пресинаптической мембраны) и поэтому препятствует встраиванию везикул в пресинаптическую мембрану. Таким образом уменьшается выделение ацетилхолина из холинергического окончания. При ботулизме нарушается нервно-мышечная передача; в тяжелых случаях возможен паралич дыхательных мышц.
4-Аминопиридин блокирует К + -каналы пресинаптической мембраны. Это способствует деполяризации мембраны и высвобождению ацетилхолина. 4-Аминопиридин облегчает нервно-мышечную передачу.
Антихолинэстеразные вещества ингибируют ацетилхолинэстеразу и таким образом препятствуют расщеплению ацетилхолина; холинергическая передача активируется.
Вещества, стимулирующие холинорецепторы, называют холиномиметиками (от греч. mimesis - подражание; эти вещества в своем действии «подражают» ацетилхолину).
Вещества, которые блокируют холинорецепторы, называют холиноблокаторами.
Гемихолиний препятствует обратному нейрональному захвату ацетилхолина.
А. Средства, стимулирующие холинергические синапсы
Из средств, стимулирующих холинергические синапсы, в медицинской практике применяют вещества, которые стимулируют холинорецепторы - холиномиметики, а также антихолинэстеразные средства (блокируют ацетилхолинэстеразу).
3.1. Холиномиметики (фармакология)
Холинорецепторы разных синапсов проявляют неодинаковую чувствительность к фармакологическим веществам. Холинорецепторы клеток органов и тканей в области окончаний парасимпатических нервных волокон проявляют повышенную чувствительность к возбуждающему действию мускарина (алкалоид грибов мухоморов). Эти холинорецепторы обозначают какМ-холинорецепторы (мускариночувствительные холинорецепторы).
Остальные холинорецепторы эфферентной иннервации проявляют высокую чувствительность к стимулирующему действию никотина ( Nicotine ; алкалоид табака), поэтому их называют N -холинорецепторами (никотиночувствительные холинорецепторы). Различают 2 типа N -холинорецепторов: N N -холинорецепторы и N м -холинорецепторы (рис. 11).

Рис. 11. Локализация хопинорецепторов.
Адр- адреналин; НА- норадреналин; М- М-холинорецепторы; N N - N -холинорецепторы нейронального типа; N M - N
К N N -холинорецепторам относят ганглионарные N -холинорецеп-торы ( N -холинорецепторы нейронов симпатических и парасимпатических ганглиев), а также N-холинорецепторы хромаффинных клеток мозгового вещества надпочечников, которые выделяют адреналин и норадреналин. Такие же рецепторы находятся в каротидных клубочках (расположены в местах деления общих сонных артерий); при их стимуляции рефлекторно возбуждаются дыхательный и сосудодвигательный центры продолговатого мозга.
К N M -холинорецепторам относят N -холинорецепторы скелетных мышц.
Как М-холинорецепторы, так и N -холинорецепторы имеются также в ЦНС.
В соответствии с делением холинорецепторов на М- и N -холинорецепторы холиномиметики делят на М-холиномиметики, N -холиномиметики и М, N -холиномиметики (стимулируют и М-, и N -холинорецепторы).
3.1.1. М-холиномиметики (фармакология)
Различают подтипы М-холинорецепторов - М 1 -, М 2 - и М 3 -холинорецепторы.
В ЦНС, в энтерохромаффиноподобных клетках желудка локализованы M 1 -холинорецепторы; в сердце - М 2 -холинорецепторы, в гладких мышцах внутренних органов, железах и в эндотелии сосудов - М 3 -холинорецепторы (табл. 1).
При возбуждении М,-холинорецепторов и М 3 -холинорецепто-ров через G -белки активируется фосфолипаза С; образуется ино-зитол-1,4,5-трифосфат, который способствует высвобождению Са 2+
Таблица 1. Локализация подтипов М-холинорецепторов
|
М 1 , |
M 2 |
М 3 |
|
|
цнс |
|||
|
Кардиомиоциты |
|||
|
Эндотелий кровеносных сосудов 1 |
|||
|
Гладкие мышцы бронхов, ЖКТ |
|||
|
Слюнные, бронхиальные, потовые железы |
|||
|
Энтерохромаффиноподобные клетки желудка |
1 При стимуляции М 3 -холинорецепторов эндотелия кровеносных сосудов высвобождается эндотелиальный релаксирующий фактор - N0, который расширяет кровеносные сосуды из саркоплазматического (эндоплазматического) ретикулума. Повышается уровень внутриклеточного Са 2+ , развиваются возбудительные эффекты.
При стимуляции М 2 -холинорецепторов сердца через G .-белки угнетается аденилатциклаза, снижаются уровень цАМФ, активность протеинкиназы и уровень внутриклеточного Са 2+ . Кроме того, при возбуждении М 2 -холинорецепторов через G о -белки активируются К + -каналы, развивается гиперполяризация клеточной мембраны. Все это ведет к развитию тормозных эффектов.
М 2 -холинорецепторы имеются на окончаниях постганглионар-ных парасимпатических волокон (на пресинаптической мембране); при их возбуждении выделение ацетилхолина уменьшается.
Мускарин стимулирует все подтипы М-холинорецепторов.
Через гематоэнцефалический барьер мускарин не проникает и поэтому на ЦНС существенного влияния не оказывает.
В связи со стимуляцией М 1 -холинорецепторов энтерохромаффиноподобных клеток желудка мускарин увеличивает выделение гистамина, который стимулирует секрецию хлористоводородной кислоты париетальными клетками.
В связи со стимуляцией М 2 -холинорецепторов мускарин урежает сокращения сердца (вызывает брадикардию) и затрудняет атриовентрикулярную проводимость.
В связи со стимуляцией М 3 -холинорецепторов мускарин:
1) суживает зрачки (вызывает сокращение круговой мышцы радужки);
2) вызывает спазм аккомодации (сокращение ресничной мышцы ведет к расслаблению цинновой связки; хрусталик становится более выпуклым, глаз устанавливается на ближнюю точку видения);
3) повышает тонус гладких мышц внутренних органов (бронхи, желудочно-кишечный тракт и мочевой пузырь), за исключением сфинктеров;
4) увеличивает секрецию бронхиальных, пищеварительных и потовых желез;
5) снижает тонус кровеносных сосудов (большинство сосудов не получает парасимпатической иннервации, но содержит неиннер-вируемые М 3 -холинорецепторы; стимуляция М 3 -холинорецепторов эндотелия сосудов ведет к высвобождению NО, который расслабляет гладкие мышцы сосудов).
В медицинской практике мускарин не применяется. Фармакологическое действие мускарина может проявляться при отравлении мухоморами. Отмечаются сужение зрачков глаз, сильное слюнотечение и потоотделение, чувство удушья (усиленная секреция бронхиальных желез и повышение тонуса бронхов), брадикардия, снижение артериального давления, спастические боли в животе, рвота, диарея.
В связи с действием других алкалоидов мухоморов, обладающих М-холиноблокирующими свойствами, возможно возбуждение ЦНС: беспокойство, бред, галлюцинации, судороги.
При лечении отравлений мухоморами проводят промывание желудка, дают солевое слабительное. Для ослабления действия мускарина вводят М-холиноблокатор атропин. Если преобладают симптомы возбуждения ЦНС, атропин не используют. Для уменьшения возбуждения ЦНС применяют препараты бензодиазепинов (диазепам и др.).
Из М-холиномиметиков в практической медицине используют пилокарпин, ацеклидин и бетанехол.
Пилокарпин - алкалоид растения, произрастающего в Южной Америке. Препарат применяют в основном местно в глазной практике. Пилокарпин суживает зрачки и вызывает спазм аккомодации (увеличивает кривизну хрусталика).
Сужение зрачков (миоз) наступает в связи с тем, что пилокарпин вызывает сокращение круговой мышцы радужной оболочки (иннервируется парасимпатическими волокнами).
Пилокарпин увеличивает кривизну хрусталика. Это связано с тем, что пилокарпин вызывает сокращение ресничной мышцы, к которой прикрепляется циннова связка, растягивающая хрусталик. При сокращении ресничной мышцы циннова связка расслабляется и хрусталик принимает более выпуклую форму. В связи с увеличением кривизны хрусталика увеличивается его преломляющая способность, глаз устанавливается на ближнюю точку видения (человек хорошо видит близкие предметы и плохо - дальние). Такое явление называют спазмом аккомодации. При этом возникает мак-ропсия (видение предметов в увеличенном размере).
В офтальмологии пилокарпин в виде глазных капель, глазной мази, глазных пленок применяют при глаукоме - заболевании, которое проявляется повышением внутриглазного давления и может вести к нарушениям зрения.
Призакрытоуголъной форме глаукомы пилокарпин снижает внутриглазное давление за счет сужения зрачков и улучшения доступа внутриглазной жидкости в угол передней камеры глаза (между радужкой и роговицей), в котором расположена гребешковая связка (рис. 12). Через крипты между трабекулами гребешковой связки (фонтановы пространства) происходит отток внутриглазной жидкости, которая далее поступает в венозный синус склеры - шлеммов канал (трабекуло-каналикулярный отток); повышенное внутриглазное давление снижается. Миоз, вызываемый пилокарпином, сохраняется 4-8 ч. Пилокарпин в виде глазных капель применяют 1-3 раза в день.
Приоткрытоугольной форме глаукомы пилокарпин также может улучшать отток внутриглазной жидкости за счет того, что при сокращении цилиарной мышцы напряжение передается на трабекулы гребешковой связки; при этом происходит растяжение трабекулярной сети, фонтановы пространства увеличиваются и улучшается отток внутриглазной жидкости.
Иногда пилокарпин в малых дозах (5-10 мг) назначают внутрь для стимуляции секреции слюнных желез при ксеростомии (сухость рта), вызванной лучевой терапией опухолей головы или шеи.
Ацеклидин - синтетическое соединение, менее токсичное, чем пилокарпин. Ацеклидин вводят под кожу при послеоперационной атонии кишечника или мочевого пузыря.
Бетанехол - синтетический М-холиномиметик, который применяют при послеоперационной атонии кишечника или мочевого пузыря.

Рис. 12. Строение глаза.
3.1.2. N -холиномиметики (фармакология)
N -холиномиметиками называют вещества, возбуждающие N - xo -линорецепторы (никотиночувствительные рецепторы).
N -холинорецепторы непосредственно связаны с N а + -каналами клеточной мембраны. При возбуждении N -холинорецепторов Na + -каналы открываются, вход Na + ведет к деполяризации клеточной мембраны и возбудительным эффектам.
N N -холинорецепторы находятся в нейронах симпатических и парасимпатических ганглиев, в хромаффинных клетках мозгового вещества надпочечников, в каротидных клубочках. Кроме того, N N -холинорецепторы обнаружены в ЦНС, в частности, в клетках Реншоу, которые оказывают тормозное влияние на мотонейроны спинного мозга.
N м -холинорецепторы локализованы в нервно-мышечных синапсах (в концевых пластинках скелетных мышц); при их стимуляции происходит сокращение скелетных мышц.
Никотин - алкалоид из листьев табака. Бесцветная жидкость, которая на воздухе приобретает коричневый цвет. Хорошо всасывается через слизистую оболочку полости рта, дыхательных путей, через кожу. Легко проникает через гематоэнцефалический барьер. Большая часть никотина (80-90%) метаболизируется в печени. Никотин и его метаболиты выводятся в основном почками. Период полуэлиминации ( t l /2 ) 1-1,5ч. Никотин выделяется молочными железами.
Никотин стимулирует в основном N N -холинорецепторы и в меньшей степени М м -холинорецепторы. В действии никотина на синапсы, имеющие на постсинаптической мембране N -холинорецепторы, по мере увеличения дозы выделяют 3 фазы:
1) возбуждение
2) деполяризационный блок (стойкая деполяризация постсинаптической мембраны)
3) недеполяризационный блок (связан с десен-ситизацией N -холинорецепторов).
При курении проявляется 1-я фаза действия никотина. Никотин стимулирует нейроны симпатических и парасимпатических ганглиев, хромаффинные клетки надпочечников, каротидные клубочки.
В связи с тем, что никотин одновременно стимулирует на уровне ганглиев симпатическую и парасимпатическую иннервацию, некоторые эффекты никотина непостоянны. Так, обычно никотин вызывает миоз, тахикардию, но возможны и противоположные эффекты (мидриаз, брадикардия). Никотин обычно стимулирует моторику желудочно-кишечного тракта, секрецию слюнных и бронхиальных желез.
Постоянным эффектом никотина является его сосудосуживающее действие (большинство сосудов получает только симпатическую иннервацию). Никотин суживает сосуды потому что:
1)стимулирует симпатические ганглии
2) увеличивает выделение адреналина и норадреналина из хромаффинных клеток надпочечников
3) стимулирует N -холинорецепторы каротидных клубочков (рефлекторно активируется сосудодвигательный центр).
В связи с сужением сосудов никотин повышает артериальное давление.
При действии никотина на ЦНС регистрируют не только возбудительные, но и тормозные эффекты. В частности, стимулируя N N - xo линорецепторы клеток Реншоу, никотин может угнетать моносинаптические рефлексы спинного мозга (например, коленный рефлекс). Угнетающее действие никотина, связанное с возбуждением тормозных клеток, возможно и в высших отделах ЦНС.
N -холинорецепторы в синапсах ЦНС могут быть локализованы как на постсинаптических, так и на пресинаптических мембранах. Действуя на пресинаптические N -холинорецепторы, никотин стимулирует высвобождение медиаторов ЦНС - дофамина, норадреналина, ацетилхолина, серотонина, β -эндорфина, а также секрецию некоторых гормонов (АКТГ, антидиуретический гормон).
У курильщиков никотин вызывает повышение настроения, приятное ощущение успокоения или активизации (зависит от типа высшей нервной деятельности). Повышает обучаемость, концентрацию внимания, бдительность, Снижает стрессовые реакции, проявления депрессии. Понижает аппетит и массу тела.
Эйфорию, вызываемую никотином, связывают с повышенным выделением дофамина, антидепрессивное действие и снижение аппетита - с выделением серотонина и норадреналина.
Курение. В сигарете содержится 6-11 мг никотина (смертельная доза никотина для человека около 60 мг). За время курения сигареты в организм курильщика попадает 1-3мг никотина. Токсическое действие никотина умеряется его быстрой элиминацией. Кроме того, к никотину быстро развивается привыкание (толерантность).
Еще больший вред при курении приносят другие вещества (около 500), которые содержатся в табачном дыме и обладают раздражающими и канцерогенными свойствами. Большинство курильщиков страдают воспалительными заболеваниями органов дыхания (ларингит, трахеит, бронхит). Рак легких у курильщиков бывает значительно чаще, чем у некурящих. Курение способствует развитию атеросклероза (никотин повышает в плазме крови уровень ЛПНП и снижает уровень ЛПВП), возникновению тромбозов, остеопорозу (особенно у женщин старше 40 лет).
Курение во время беременности приводит к снижению массы плода, повышению послеродовой смертности детей, отставанию детей в физическом и психическом развитии.
К никотину развивается психическая зависимость; при прекращении курения курильщики испытывают тягостные ощущения: ухудшение настроения, нервозность, беспокойство, напряжение, раздражиельность, агрессивность, снижение концентрации внимания, снижение познавательных способностей, депрессию, повышение аппетита и массы тела. Наиболее выражено большинство этих симптомов через 24-48 ч после прекращения курения. Затем они уменьшаются примерно в течение 2 нед. Многие курильщики, понимая вред курения, тем не менее не могут избавиться от этой вредной привычки.
Для того, чтобы уменьшить неприятные ощущения при прекращении курения, рекомендуют:
1) жевательную резинку, содержащую никотин (2 или 4 мг),
2) трансдермальную терапевтическую систему с никотином - специальный пластырь, равномерно выделяющий небольшие количества никотина в течение 24 ч (наклеивается на здоровые участки кожи),
3) мунштук, содержащий картридж с никотином и ментолом.
Указанные препараты никотина пробуют использовать в качестве лекарственных средств при болезни Альцгеймера, болезни Паркинсона, язвенном колите, синдроме Туретта (моторные и вокальные тики у детей) и некоторых других патологических состояниях.
Острое отравление никотином проявляется такими симптомами, как тошнота, рвота, диарея, боли в животе, головная боль, головокружение, потливость, нарушения зрения и слуха, дезориентация. В тяжелых случаях развивается коматозное состояние, нарушается дыхание, падает артериальное давление. В качестве лечебных мероприятий проводят промывание желудка, назначают внутрь активированный уголь, принимают меры борьбы с сосудистым коллапсом и нарушениями дыхания.
Цитизин (алкалоид термопсиса) илобелии (алкалоид лобелии) сходны по строению и действию с никотином, но менее активны и токсичны.
Цитизин в составе таблеток «Табекс» и лобелии в составе таблеток «Лобесил» применяют для облегчения отвыкания от курения.
Цититон (0,15% раствор цитизина) и раствор лобелина иногда вводят внутривенно в качестве рефлекторных стимуляторов дыхания.
3.1.3. M . N -холиномиметики (фармакология)
К М, N -холиномиметикам следует отнести прежде всегоацетилхолин - медиатор, с помощью которого передается возбуждение во всех холинергических синапсах. Выпускается лекарственный препарат ацетилхолина. В клинике препарат используют редко из-за кратковременности действия (несколько минут; препарат быстро инактивируется холинэстеразой плазмы крови и ацетилхолинэсте-разой). В то же время ацетилхолин - излюбленный препарат для экспериментальной работы; кратковременность действия позволяет вводить препарат в течение исследования многократно.
Ацетилхолин возбуждает одновременно М- и N -холинорецепторы. Преобладает действие ацетилхолина на М-холинорецепторы. Поэтому обычно проявляются «мускариноподобные» эффекты ацетилхолина. Ацетилхолин оказывает выраженное влияние на сердечно-сосудистую систему:
1) урежает сокращения сердца (отрицательное хронотропное действие);
2) ослабляет сокращения предсердий и в меньшей степени - желудочков (отрицательное инотропное действие);
3) затрудняет проведение импульсов в атриовентрикулярном узле (отрицательное дромотропное действие);
4) расширяет кровеносные сосуды.
Большинство кровеносных сосудов не получает парасимпатической иннервации, но содержит в эндотелии и в гладких мышцах неиннервируемые М 3 -холинорецепторы. При возбуждении ацетил-холином М 3 -холинорецепторов эндотелия из эндотелиальных клеток высвобождается эндотелиальный релаксирующий фактор - NО, который вызывает расширение кровеносных сосудов (при удалении эндотелия ацетилхолин суживает сосуды - стимуляция М 3 -холинорецепторов гладких мышц сосудов). Кроме того, ацетилхолин уменьшает сосудосуживающее влияние симпатической иннервации (стимулирует М 2 -холинорецепторы на окончаниях симпатических адренергических волокон и за счет этого уменьшает выделение норадреналина).
В связи с брадикардией и расширением артерий ацетилхолин в эксперименте при внутривенном введении выражение снижает артериальное давление. Но если блокировать М-холинорецепторы атропином, большие дозы ацетилхолина вызывают не снижение, а повышение артериального давления (рис. 13). На фоне блокады М-холинорецепторов проявляется «никотиноподобное» действие ацетилхолина: возбуждение симпатических ганглиев и хромаффинных клеток надпочечников (высвобождение адреналина и норадреналина, которые суживают кровеносные сосуды).
Ацетилхолин повышает тонус бронхов, стимулирует моторику кишечника, повышает тонус детрузора мочевого пузыря, увеличивает секрецию бронхиальных, пищеварительных и потовых желез.
Путем некоторого изменения структуры ацетилхолина был синтезированкарбахолин, который не разрушается ацетилхолинэсте-разой и действует более продолжительно. Растворы карбахолина иногда используют в виде глазных капель при глаукоме.

3.2. Антихолинэстеразные вещества
Антихолинэстеразные вещества получили свое название в связи со способностью ингибировать холинэстеразы. Антихолинэстеразные вещества ингибируют ацетилхолинэстеразу (фермент, гидро-лизующий ацетилхолин в холинергических синапсах) и бутирилхолинэстеразу (холинэстераза плазмы крови; псевдохолинэстераза). Ингибируя ацетилхолинэстеразу в холинергических синапсах, антихолинэстеразные вещества препятствуют гидролизу ацетилхолина и в связи с этим значительно усиливают и удлиняют действие ацетилхолина. Непосредственно на холинорецепторы антихолинэстеразные вещества либо совсем не действуют, либо это действие выражено незначительно.
Таким образом, при введении в организм антихолинэстеразных веществ все возникающие при этом эффекты обусловлены действием эндогенного ацетилхолина. При этом отмечаются: сужение зрачков глаз, спазм аккомодации, брадикардия, повышение тонуса гладких мышц внутренних органов (бронхов, желудочно-кишечного тракта, мочевого пузыря), увеличение секреции бронхиальных, пищеварительных, потовых желез. Отчетливо выражено стимулирующее влияние антихолинэстеразных веществ на нервно-мышечные синапсы, в связи с чем эти вещества повышают тонус скелетных мышц. Те антихо-линэстеразные вещества, которые легко проникают через гематоэн-цефалический барьер, оказывают возбуждающее действие на ЦНС.
Различают антихолинэстеразные вещества обратимого и необратимого действия.
Кантихолинэстеразным веществам обратимого действия относят физостигмин, неостигмин, пиридостигмин, эдрофоний, галантамин, ривастигмин, донепезил. Указанные вещества (за исключением эдрофония) обратимо связываются с анионным и эстеразным центрами ацетилхолинэстеразы и ингибируют активность фермента в течение нескольких часов. Эдрофоний взаимодействует только с анионным центром фермента и действует примерно 10 мин.
Первым антихолинэстеразным веществом, примененным в медицинской практике, былфизостигмин - алкалоид калабарских бобов, произрастающих в Западной Африке. Растворы физостигмина иногда используют в глазной практике при глаукоме в качестве средства, суживающего зрачки и улучшающего отток внутриглазной жидкости.
Неостигмин (прозерин) - синтетический антихолинэстеразный препарат; четвертичное аммониевое соединение. Действие неостигмина, как и других антихолинэстеразных веществ, связано с тем, что он ингибирует ацетилхолинэстеразу и тем самым усиливает и пролонгирует действие эндогенного ацетилхолина. Так же, как и при введении ацетилхолина, при этом преобладают эффекты, связанные с возбуждением парасимпатической иннервации. Кроме того, облегчается нервно-мышечная передача.
Препарат назначают внутрь и парентерально (под кожу, в вену). Неостигмин - полярное соединение и плохо всасывается в желудочно-кишечном тракте. Поэтому доза неостигмина для приема внутрь значительно выше, чем для парентерального введения (внутрь 0,015г, парентерально 0,0005г). Длительность действия неостигмина около 4 ч.
Фармакологические эффекты неостигмина:
1)сужение зрачков (миоз) - сокращение круговой мышцы радужки;
2)спазм акккомодации - хрусталик становится более выпуклым, так как вследствие сокращения ресничной (цилиарной) мышцы расслабляется циннова связка (ресничный поясок); глаз устанавливается на ближнюю точку видения;
3)брадикардия вследствие усиления тормозного влияния блуждающего нерва на синоатриальный узел;
4)затруднение атриовентрикулярной проводимости в связи с усилением тормозного влияния блуждающего нерва на атриовентрикулярный узел;
5)повышение тонуса гладких мышц внутренних органов (бронхи, желудочно-кишечный тракт, мочевой пузырь, матка);
6)увеличение секреции экзокринных желез (слюнные, бронхиальные железы, железы желудка и кишечника, потовые железы);
7)облегчение нервно-мышечной передачи - усиление сокращений скелетных мышц.
Показания к применению неостигмина
1.Миастения - аутоиммунное заболевание, при котором образуются аутоантитела к N м -холинорецепторам скелетных мышц, уменьшается количество N м -холинорецепторов и нарушается нервно-мышечная передача.
Заболевание проявляется слабостью скелетных мышц. В первую очередь снижается тонус экстраокулярных мышц, мышц лица, глотки, гортани. Развиваются птоз (опущение век), диплопия, нарушение жевания, а также дисфагия и дизартрия. В тяжелых случаях возможно ослабление сократимости мышц шеи, конечностей; при миастеническом кризе может быть нарушение дыхания из-за слабости дыхательных мышц.
Неостигмин при миастении оказывает симптоматическое действие, восстанавливая на время нервно-мышечную передачу. Препарат назначают внутрь, а при миастеническом кризе (сильная мышечная слабость, нарушение глотания, дыхания) - под кожу или внутримышечно.
Для устранения мускариноподобных эффектов неостигмина предварительно вводят М-холиноблокатор атропин. Не рекомендуют вводить неостигмин и атропин одновременно, так как атропин сначала может вызывать брадикардию.
2.В качестве антагониста курареподобных средств антидеполяризующего конкурентного действия.
3.Послеоперационная атония кишечника или мочевого пузыря. Препарат вводят под кожу или внутримышечно.
4.Глаукома; применяют редко
Побочные эффекты неостигмина: миоз, спазм аккомодации, увеличение секреции слюнных и бронхиальных желез, бронхоспазм, тошнота, рвота, диарея, спастические боли в животе, артериальная гипотензия, аллергические реакции. При передозировке неостигмина возможно развитие холинергического криза, который по симптомам сходен с миастеническим кризом (нарушение нервно-мышечной передачи, мышечная слабость).
Пиридостигмин (местинон) сходен по действию с неостигмином. Применяется при миастении. Действует более продолжительно - около 6 ч; мускариноподобные эффекты менее выражены.
Эдрофоний (тензилон) при внутривенном введении действует через 30-60 с; продолжительность действия около 10 мин. Эдрофоний применяют для диагностики миастении, а также для дифференцировки миастенического и холинергического кризов (холинергический криз может быть связан с передозировкой антихолинэстеразных средств и, как и миастенический криз, проявляется слабостью скелетных мышц). При миастеническом кризе эдрофоний проявляет терапевтический эффект; при холинергическом кризе нервно-мышечная передача ухудшается, однако действие эдрофония быстро проходит.
При мышечных параличах, связанных с нарушениями ЦНС, например, при параличах после полиомиелита, применяютгалантамин (нивалин), хорошо проникающий через гематоэнцефалический барьер.
Кроме того, галантамин используют при атонии кишечника и мочевого пузыря, при миастении, в качестве антагониста курареподобных средств антидеполяризующего конкурентного действия.
Галантамин был одним из первых антихолинэстеразных средств, которые стали применять при болезни Альцгеймера. При этом заболевании применяют такжеривастигмин (экселон).
Однако в настоящее время наиболее эффективным препаратом при болезни Альцгеймера считаютдонепезил, который избирательно ингибирует ацетилхолинэстеразуЦНС, мало влияя на периферическую ацетилхолинэстеразу.
Противопоказаниями к назначению антихолинэстеразных средств являются эпилепсия, болезнь Паркинсона, бронхиальная астма, стенокардия, нарушения проводящей системы сердца.
Кантихолинэстеразным средствам необратимого действия относятся фосфорорганические соединения (ФОС). В отличие от указанных выше антихолинэстеразных веществ ФОС на длительное время инактивируют ацетилхолинэстеразу. При этом происходит «старение» фермента и его инактивация становится практически необратимой.
ФОС отличаются высокой токсичностью. Некоторые из этих веществ используют в качестве инсектицидных средств. Так, в качестве инсектицидов применяются карбофос, тиофос и др. Эти вещества в связи с их широким применением в быту нередко бывают причиной отравлений (отравления возможны даже при попадании этих веществ на кожу, так как они легко всасываются через кожную поверхность).
Отравления фосфорорганическими соединениями проявляются такими симптомами, как миоз, потливость, слюнотечение, удушье (бронхоспазм и увеличение секреции бронхиальных желез), бради-кардия, а затем тахикардия, снижение, а затем повышение артериального давления, психомоторное возбуждение, рвота, спастические боли в животе. В более тяжелых случаях это сопровождается мышечными подергиваниями и судорогами; возбуждение сменяется заторможенностью, артериальное давление падает, развивается коматозное состояние; смерть наступает от паралича дыхательного центра.
Большинство этих симптомов связано с возбуждением парасимпатической иннервации. Поэтому при отравлениях фосфорорганическими соединениями прежде всего назначают вещества, блокирующие парасимпатическую иннервацию. Обычно применяют М-холиноблокаторы, чаще всего атропин, который в этих случаях вводят внутривенно в больших дозах (2-4 мл 0,1% раствора) и при необходимости повторяют введение. Кроме того, назначаютреактиваторы холинэстеразы, которые при их применении в первые часы после отравления восстанавливают активность ингибированной ацетилхолинэстеразы. К таким препаратам относятсятримедоксим (дипироксим) иизонитрозин. При отравлениях антихолинэстеразными средствами обратимого действия (физостигмин, неостигмин и др.) эти вещества неэффективны.
При повышении артериального давления (может быть связано с активацией симпатической иннервации и центральным действием ФОС) применяют гипотензивные средства. Дополнительными мероприятиями являются дача кислорода и, при необходимости, искусственное дыхание. При попадании фосфорорганических соединений на кожу надо вытереть ее сухим тампоном, а затем вымыть 5-6% раствором натрия гидрокарбоната и теплой водой с мылом.
Б. Средства, блокирующие холинергические синапсы
3.3. Вещества, уменьшающие высвобождение ацетилхолина
Ботулиновый токсин вызывает протеолиз синаптобревина (белок мебраны везикул, взаимодействующий с белками пресинаптической мембраны) и поэтому препятствует экзоцитозу везикул с ацетилхолином. Лекарственный препарат ботулинового токсина - ботокс применяют при блефароспазме, спастической кривошее. Препарат вводят в спазмированные мышцы, после чего наступает их длительное расслабление.
Ботокс используют также в косметических целях. При введении препарата в мышцы лица происходят их расслабление и разглаживание морщин.
Частная фармакология
1. Схема строения и функциональная роль периферической нервной системы. Передача возбуждения в холинергических и адренергических синапсах.
эффекты, вызванные повышением активности симпатического отдела
автономной нервной системы:
Радужка – сокращение радиальной мышцы ( 1 -Ар)
Цилиарная мышца – расслабляется (-Ар)
2) сердце:
Синоатриальный узел, эктопические пейсмейкер – ускорение ( 1 -Ар)
Сократимость – повышается ( 1 -Ар)
3) ГМК сосудов:
Кожа, сосуды внутренних органов – сокращаются (-Ар)
Сосуды скелетных мышц – расслабляются ( 2 -Ар)
4) бронхиолярные ГМК: расслабляются ( 2 -Ар)
ГМК стенок – расслабляются ( 2 , 2 -Ар)
ГМК сфинктеров – сокращаются ( 1 -Ар)
Мышечное сплетение – угнетается (-Ар)
6) ГМК мочеполовой системы:
Стенки мочевого пузыря – расслабляются ( 2 -Ар)
Сфинктер – сокращается ( 1 -Ар)
Матка при беременности – расслабляется ( 2 -Ар) или сокращается (-Ар)
Пенис, семенные пузырьки – эякуляция (-Ар)
Пиломоторные ГМК - сокращаются (-Ар)
Потовые железы: терморегуляторные – активация (М-Хр), апокриновые – активация (-Ар)
8) метаболические функции:
Печень: глюконеогенез и глюкогенолез (/ 2 -Ар)
Жировые клетки: липолиз ( 3 -Ар)
Почки: выделение ренина ( 1 -Ар)
эффекты, обусловленные повышением тонуса парасимпатического отдела
автономной нервной системы.
Радужка – сокращение циркулярной мышцы (М 3 -Хр)
Цилиарная мышца – сокращается (М 3 -Хр)
2) сердце:
Синоатриальный узел – замедляется (М 2 -Хр)
Сократимость – замедляется (М 2 -Хр)
3) ГМК сосудов:
Эндотелий – выделение эндотелиального релаксирующего фактора NO (М 3 -Хр)
4) бронхиолярные ГМК: сокращаются (М 3 -Хр)
ГМК стенок – сокращаются (М 3 -Хр)
ГМК сфинктеров – расслабляются (М 3 -Хр)
Секреция – повышается (М 3 -Хр)
Мышечное сплетение – активируется (М 1 -Хр)
6) ГМК мочеполовой системы:
Стенки мочевого пузыря – сокращаются (М 3 -Хр)
Сфинктер – расслабляются (М 3 -Хр)
Матка при беременности –сокращается (М 3 -Хр)
Пенис, семенные пузырьки – эрекция (М-Хр)
строение холинергического синапса.

В холинэргических синапсах передача возбуждения осуществляется посредством ацетилхолина. АцХ синтезируется в цитоплазме окончаний холинэргических нейронов. Он образуется из холина и АцКоА при участии цитоплазматического энзима холинацетилазы. Депонируется он в синаптических пузырьках (везикулах). Нервные импульсы вызывают высвобождение АцХ в синаптическую щель, после чего он взаимодействует с холинорецепторами. Структура ХР не установлена. По имеющимся данным, ХР имеет 5 белковых субъединиц (,,,), окружающих ионный (натриевый) канал и проходящий через всю толщу липидной мембраны. АцХ взаимодействует с -субъединицами, что приводит к открыванию ионного канала и деполяризации постсинаптической мембраны.
ХР бывают: мускариночувствительные и никотиночувствительные. МХР расположены в постсинаптической мембране клеток эффекторных органов у окончаний постганглионарных парасимпатических волокон, а также на нейронах вегетативных ганглиев и в ЦНС (в коре, ретикулярной формации). Есть м 1 -ХР (в вегетативных ганглиях, ЦНС), м 2 -ХР (сердце), м 3 -ХР (гладкие мышцы, экзокринные железы). НХР находятся в постсинаптической мембране ганглионарных нейронов у окончаний всех преганглионарных волокон, мозговом веществе надпочечников, синокаротидной зоне, концевых пластинках скелетных мышц, ЦНС. Эффекты возбуждения ПНС: сердце (брадикардия, снижение сократимости, возбудимости, проводимости, понижение АД); бронхи (бронхоспазм, повышение секреции бронхиальных желёз); глаз (сужение зрачка, понижение внутриглазного давления, спазм аккомодации); сфинктеры (понижение тонуса); гладкие мышцы (повышение тонуса и перистальтики ЖКТ, повышение тонуса мочевого пузыря); железы (повышение секреции желёз ЖКТ, гиперсаливация слюнных желёз). Эффекты возбуждения СНС: сердце (тахикардия, повышение сократимости, возбудимости, повышение АД); бронхи (расширение, понижение секреции желёз); глаз (расширение зрачка, повышение внутриглазного давления, паралич аккомодации); гладкие мышцы (снижение тонуса, перистальтики ЖКТ); сфинктеры (повышение тонуса); железы (понижение секреции).
Классификация ХЭ средств:
Холиномиметики делятся на М- и Н- (бывают: 1.прямого (ацетилхолин, карбохолин) и 2.непрямого (обратимого действия (прозерин, галантамин,изостегмин, оксазил) и необратимого действия) действия ; М (пилокарпина гидрохлорид, ацеклидин); Н (никотин, лобелин, цититон, анабазин).
Холиноблокаторы делятся на М- и Н- (1.центрального (амизил, циклодол, тропацин) и 2.периферического (спазмолитин, апрофен) действия ), М (атропин, платифиллин, скопаламин, метацин, гастрозепин, тровентол), Н (1.ганглиоблокаторы (бензогексоний, арфонад, пентамин, гигроний; 2.миорелаксанты ; 3.курареподобные средства (деполяризующие (дитилин); антидеполяризующие (тубокурарина гидрохлорид, панкуроний, пиперкуроний); смешанного действия (диоксоний)).
строение адренергического синапса.

В адренергических синапсах передача возбуждения осуществляется посредством норадреналина. В пределах периферической иннервации норадреналин принимает участие в передаче импульсов с адренергических волокон на эффекторные клетки. Адренэргические аксоны, подходя к эффектору, разветвляются на тонкую сеть волокон с варикозными утолщениями, выполняющими функцию нервных окончаний, которые участвуют в образовании синаптических контактов с эффекторными клетками. В варикозных утолщениях находятся везикулы (пузырьки), содержащие медиатор норадреналин. Биосинтез норадреналина осуществляется в адренергических нейронах из тирозина с участием ряда энзимов. Образование ДОФА и дофамина происходит в цитоплазме нейронов, а норадреналина в везикулах. В ответ на нервные импульсы происходит высвобождение норадреналина в синаптическую щель и последующее взаимодействие его с адренорецепторами постсинаптической мембраны.
Различают и -адренорецепторы.
Сосуды кожи, почек, кишечника ( 1 и 2) - при их стимуляции - сокращение мышц, сужение сосудов.
Сосуды скелетных мышц, печени, коронарные сосуды ( 2) - расширение.
Вены ( 1) - сужение.
Сердце ( 1) - повышение ЧСС, силы сердечных сокращений, повышение проводимости, возбудимости миокарда, повышение потребности миокарда в кислороде).
Бронхи ( 2) - расширение.
Глаз (радиальная мышца) ( 1) - мидриаз, снижение ВГД.
Кишечник и мускулатура ( 1) - расслабление, снижение тонуса, перистальтики.
Сфинктеры кишечника ( 1) - сокращение сфинктеров.
Матка (миометрий) ( 2) - снижение тонуса.
Шейка матки ( 1) - сокращение.
Простата, сфинктеры мочевого пузыря, простатическая часть уретры ( 1) - повышение тонуса, эякуляция.
Почки (юкстагломерулярный аппарат) ( 1 и 2) - повышение секреции ренина.
Капсула селезёнки ( 1) - сокращение.
Тромбоциты ( 2 и 2) - соответственно повышение и понижении агрегации.
-клетки поджелудочной железы ( 1) - понижение секреции инсулина.
Депо гликогена ( 2) - гликогенолиз.
Жировые депо ( 3) - липолиз и термогенез в жировой ткани.
Классификация средств, влияющих на адренэргические синапсы.
Делятся на адреномиметики и адреноблокаторы.
Адреномиметики бывают прямого и непрямого действия. Прямого действия бывают: (адреналин - все виды рецепторов, норадреналин - все, кроме 2); (мезатон - 1 , нафтизин, глазолин - 2); (изодрин - 1 , 2 , добутамин - 1 , тербутамин - 2 , сальбутамол - 2). Непрямого действия, или симпатомиметики (фенамин, эфедрина гидрохлорид).
Адреноблокаторы бывают: непрямого и прямого действия. Непрямого действия или симпатолитики (резерпин, октадин, орнид). Прямого действия: (лабетолол - 1 , 1 , 2); (фентоламин - 1 , 2 , тропафен - 1 , 2 , празозин - 1); (анаприлин - 1 , 2 , окспренолол - 1 , 2 , атенолол - 1).
Мышечную и железистую клетку передается посредством специального структурного образования — синапса.
Синапс — структура, обеспечивающая проведение сигнала от одной к другой. Термин был введен английским физиологом Ч. Шеррингтоном в 1897 г.
Строение синапса
Синапсы состоят из трех основных элементов: пресинаптической мембраны, постсинаптической мембраны и синаптической щели (рис. 1).
Рис. 1. Строение синапса: 1 — микротрубочки; 2 — митохондрии; 3 — синаптические пузырьки с медиатором; 4 — пресинаптическая мембрана; 5 — постсинаптическая мембрана; 6 — рецепторы; 7 -синаптическая щель
Некоторые элементы синапсов могут иметь и другие названия. Например, синаптическая бляшка — это синапс между , концевая пластинка — постсинаптическая мембрана , моторная бляшка — пресинаптическое окончание аксона на мышечном волокне.

Пресинаптическая мембрана покрывает расширенное нервное окончание, которое представляет собой нейросекреторный аппарат. В пресинаптической части находятся пузырьки и митохондрии, обеспечивающие синтез медиатора. Медиаторы депонируются в гранулах (пузырьках).
Постсинаптическая мембрана - утолщенная часть мембраны клетки, с которой контактирует пресинаптическая мембрана. Она имеет ионные каналы и способна к генерации потенциала действия. Кроме того, на ней расположены специальные белковые структуры — рецепторы, воспринимающие действие медиаторов.
Синаптическая щель представляет собой пространство между пресинаптической и постсинаптической мембранами, заполненное жидкостью, близкой по составу к .

Рис. Строение синапса и процессы, осуществляемые в ходе синаптической передачи сигнала
Виды синапсов
Синапсы классифицируются по местоположению, характеру действия, способу передачи сигнала.
По месту положения выделяют нервно-мышечные синапсы, нервно-железистые и нейро-нейрональные; последние, в свою очередь, делятся на аксо-аксональные, аксо-дендритические, аксо-соматические, дендро-соматические, дендро-дендротические.
По характеру действия на воспринимающую структуру синапсы могут быть возбуждающими и тормозящими.
По способу передачи сигнала синапсы делятся на электрические, химические, смешанные.
Таблица 1. Классификация и виды синапсов

Классификация синапсов и механизм передачи возбуждения
Синапсы классифицируют следующим образом:
- по местоположению — периферические и центральные;
- по характеру их действия — возбуждающие и тормозящие;
- по способу передачи сигналов — химические, электрические, смешанные;
- по медиатору, с помощью которого осуществляется передача, — холинергические, адренергические, серотонинергические и т.д.
В возбуждение передается с помощью медиаторов (посредников).
Медиаторы — молекулы химических веществ, которые обеспечивают передачу возбуждения в синапсах. Другими словами химические вещества, участвующие в передаче возбуждения или торможения от одной возбудимой клетки к другой.
Свойства медиаторов
- Синтезируются в нейроне
- Накапливаются в окончании клетки
- Выделяются при появлении иона Са2+ в пресинаптическом окончании
- Оказывают специфическое действие на постсинаптическую мембрану
По химическому строению медиаторы можно подразделить на амины (норадреналин, дофамин, серотонин), аминокислоты (глицин, гамма-аминомасляная кислота) и полипептиды (эндорфины, энкефалины). Ацетилхолин известен в основном как возбуждающий медиатор и содержится в различных отделах ЦНС. Медиатор находится в пузырьках пресинаптического утолщения (синаптической бляшки). Медиатор синтезируется в клетках нейрона и может ресинтезироваться из метаболитов его расщепления в синаптической щели.
При возбуждении терминалей аксона происходит деполяризация мембраны синаптической бляшки, вызывающая поступление ионов кальция из внеклеточной среды внутрь нервного окончания через кальциевые каналы. Ионы кальция стимулируют перемещение синаптических пузырьков к пресинаптической мембране, их слияние с ней и последующий выход медиатора в синаптическую щель. После проникновения в щель медиатор диффундирует к постсинаптической мембране, содержащей на своей поверхности рецепторы. Взаимодействие медиатора с рецепторами вызывает открытие натриевых каналов, что способствует деполяризации постсинаптической мембраны и возникновению возбуждающего постсинаптического потенциала. В нервно-мышечном синапсе этот потенциал называется потенциалом концевой пластинки. Между деполяризованной постсинаптической мембраной и соседними с ней поляризованными участками этой же мембраны возникают местные токи, которые деполяризуют мембрану до критического уровня с последующей генерацией потенциала действия. Потенциал действия распространяется по всем мембранам, например, мышечного волокна и вызывает его сокращение.
Выделившийся в синаптическую щель медиатор связывается с рецепторами постсинаптической мембраны и подвергается расщеплению соответствующим ферментом. Так, холинэстераза разрушает медиатор ацетилхолин. После этого некоторое количество продуктов расщепления медиатора поступает в синаптическую бляшку, где из них снова ресинтезируется ацетилхолин.
В организме имеются не только возбуждающие, но и тормозные синапсы. По механизму передачи возбуждения они сходны с синапсами возбуждающего действия. В тормозных синапсах медиатор (например, гамма-аминомасляная кислота) связывается с рецепторами постсинаптической мембраны и способствует открытию в ней . При этом активизируется проникновение этих ионов внутрь клетки и развивается гиперполяризация постсинаптической мембраны, обусловливающая возникновение тормозного постсинаптического потенциала.
В настоящее время выяснено, что один медиатор может связываться с несколькими различными рецепторами и индуцировать различные реакции.
Химические синапсы
Физиологические свойства химических синапсов
Синапсы с химической передачей возбуждения обладают определенными свойствами:
- возбуждение проводится в одном направлении, так как медиатор выделяется только из синаптической бляшки и взаимодействует с рецепторами на постсинаптической мембраны;
- распространение возбуждения через синапсы происходит медленнее, чем по нервному волокну (синаптическая задержка);
- передача возбуждения осуществляется с помощью специфических медиаторов;
- в синапсах изменяется ритм возбуждения;
- синапсы способны утомляться;
- синапсы обладают высокой чувствительностью к различным химическим веществам и гипоксии.
Одностороннее проведение сигнала. Сигнал передается только от пресинаптической мембраны к постсинаптической. Это вытекает из особенностей строения и свойств синаптических структур.
Замедленная передача сигнала. Обусловлена синаптической задержкой в передаче сигнала с одной клетки на другую. Задержка вызывается временными затратами на процессы выброса медиатора, его диффузии к постсинаптической мембране, связывания с рецепторами постсинаптической мембраны, деполяризации и преобразования постсинаптического потенциала в ПД (потенциал действия). Длительность синаптической задержки колеблется от 0,5 до 2 мс.
Способность к суммации эффекта от приходящих к синапсу сигналов. Такая суммация проявляется, если последующий сигнал приходит к синапсу через короткое время (1- 10 мс) после предыдущего. В таких случаях амплитуда ВПСП возрастает и на постсинаптическом нейроне может генерироваться большая частота ПД.
Трансформация ритма возбуждении. Частота нервных импульсов, приходящих к пресинаптической мембране, обычно не соответствует частоте ПД, генерируемых постсинаптическим нейроном. Исключение составляют синапсы, передающие возбуждение с нервного волокна на скелетную мышцу.
Низкая лабильность и высокая утомляемость синапсов. Синапсы могут проводить 50-100 нервных импульсов в секунду. Это в 5-10 раз меньше, чем максимальная частота ПД, которую могут воспроизводить нервные волокна при их электростимуляции. Если нервные волокна считаются практически неутомляемыми, то в синапсах утомление развивается весьма быстро. Это происходит из-за истощения запасов медиатора, энергетических ресурсов, развития стойкой деполяризации постсинаптической мембраны и т.д.
Высокая чувствительность синапсов к действию биологически активных веществ, лекарственных препаратов и ядов. Например, яд стрихнин блокирует функцию тормозных синапсов ЦНС, связываясь с рецепторами, чувствительными к медиатору глицину. Столбнячный токсин блокирует тормозные синапсы, нарушая выделение медиатора из пресинаптической терминали. В обоих случаях развиваются опасные для жизни организма явления. Примеры действия биологически активных веществ и ядов на передачу сигналов в нервно-мышечных синапсах рассмотрены выше.
Свойства облегчения и депрессии синоптической передачи. Облегчение синаптической передачи имеет место, когда нервные импульсы поступают к синапсу через короткое время (10-50 мс) друг за другом, т.е. достаточно часто. При этом в течение некоторого промежутка времени каждый последующий ПД, приходящий к пресинаптической мембране, вызывает увеличение содержания медиатора в синаптической щели, возрастание амплитуды ВПСП и увеличение эффективности синаптической передачи.
Одним из механизмов облегчения является накопление ионов Са 2 в пресинаптической терминали. Для удаления кальциевым насосом порции кальция, вошедшей в синаптическую терминаль при поступлении ПД, необходимо несколько десятков миллисекунд. Если в это время приходит новый потенциал действия, то новая порция кальция входит в терминаль и ее эффект на высвобождение нейромедиатора складывается с остаточным количеством кальция, которое кальциевый насос не успел удалить из нейроплазмы терминали.
Имеются и другие механизмы развития облегчения. Этот феномен в классических руководствах по физиологии называют также посттетанической потенциацией. Облегчение синаптической передачи имеет значение в функционировании механизмов памяти, для образования условных рефлексов и обучения. Облегчение передачи сигналов лежит в основе развития пластичности синапсов и улучшения их функций при частой активации.
Депрессия (угнетение) передачи сигналов в синапсах развивается при поступлении очень частых (для нервно-мышечного синапса более 100 Гц) нервных импульсов к пресинаптической мембране. В механизмах развития явления депрессии имеют значение истощение запасов медиатора в пресинаптической терминали, снижение чувствительности рецепторов постсинаптической мембраны к медиатору, развитие стойкой деполяризации постсинаптической мембраны, затрудняющих генерацию ПД на мембране постсинаптической клетки.
Электрические синапсы
Кроме синапсов с химической передачей возбуждения в организме есть синапсы с электрической передачей. Эти синапсы имеют очень узкую синаптическую щель и пониженное электрическое сопротивление между двумя мембранами. Благодаря наличию поперечных каналов между мембранами и низкому сопротивлению, электрический импульс легко проходит через мембраны. Электрические синапсы обычно характерны для однотипных клеток.
В результате воздействия раздражителя пресинаптический потенциал действия раздражает постсинаптическую мембрану, где возникает распространяющийся потенциал действия.
Характеризуются большей скоростью проведения возбуждения по сравнению с химическими синапсами и низкой чувствительностью к воздействию химических веществ.
Электрические синапсы бывают с одно- и двусторонней передачей возбуждения.
В организме встречаются и электрические тормозные синапсы. Тормозное влияние развивается за счет действия тока, который вызывает гиперполяризацию постсинаптической мембраны.
В смешанных синапсах может происходить передача возбуждения с помощью как электрических импульсов, так и медиаторов.
Холинергические синапсы представлены более широко.
Работа холинергического синапса.
Медиатор – ацетилхолин. Ацетилхолин синтезируется во всех нервных окончаниях(холинергических) из аминоспирта холина и предварительно активированного ацетата – ацилКоА под действием фермента – ацетилхолинэстеразы. Ацетилхолин синтезируется в везикулах нервных окончаний. Эти везикулы увеличиваются в размерах, подходя к пресинаптической мембране. Большие содержат готовый ацетилхолин.
Ацетилхолин, выделившийся в синаптическую щель, взаимодействует с холинорецепторами на постсинаптической мембране.
Рецепторы делятся на:
1.м – холинорецепторы(возбуждаются алкалоидом из мухомора – мускарином и блокируется алкалоидом атропином)
2.н – холинорецепторы(возбуждаются малыми дозами никотина и блокируются большими дозами никотина).
Н – холинорецепторы – на скелетной мускулатуре(Н м - холинорецепторы), в ганглиях(Н н - холинорецепторы). На исполнительных органах парасимпатики – М – холинорецепторы.
М – холинорецепторы делятся на 3 подтипа: М 1 , М 2 , М 3 .
М 1 – локализованы в ЦНС и их возбуждение – кратковременная память. В вегетативных ганглиях(модулирующая роль) париетальных клеток желудка.
М 2 – их возбуждение связано с торможением функции любого органа, на котором они расположены(в основном сердце).
М 3 – расположены в гладких мышцах и железах. Все эффекты, связанные с их возбуждением – связаны с усилением функции органов(но сфинктеры расслабляются). Железы усиливают секрецию.
Механизм функционирования М – рецепторов.
М 1 и М 3 – рецепторы через G q – белок связаны с фосфолипазой С, то есть при их возбуждении идет наработка инозитолтрифосфата и диацилглицерина, следовательно идет повышение концентрации свободного кальция, то есть повышается тонус мышц.
М 2 – связаны через G i – белок с аденилатциклазой или ионными каналами. Их возбуждение приведет к уменьшению активности аденилатциклазы, повышению проводимости, что приводит к выходу калия из клетки, то есть возникает гиперполяризация, и как следствие снижение функции.
Н – холинорецепторы не разделены на подтипы, а по локализации делятся на:
1.никотиновые мышечного типа(Н м). Находятся на скелетных мышцах
2.нейронального типа(Н н). Локализация: в ганглиях(как симпатики, так и парасимпатики) – эффект возбуждения – усиление проводимости; в мозговом слое надпочечников – эффект – усиление выделения адреналина; каротидный клубочек – возбуждение приводит к рефлекторной активации дыхания в ЦНС.
Механизм действия.
Н – рецепторы представляют собой натриевый ионный канал(5 субъединиц - 2α, β, γ, δ). Вещество, взаимодействующее с этим рецептором, взаимодействует с α – субъединицей, которые формируют натриевый канал. При его возбуждении входящий ток натрия, то есть идет деполяризация, следствием становится сокращение мышцы.
Второй этап работы синапса: после того как ацетилхолин провзаимодействовал с рецепторами, он подвергается действию фермента – ацетилхолинэстеразы(разрушается). Реакция очень быстрая.
Аминоспирт холин, который образовался в результате разрушения ацетилхолина в синаптической щели, подвергается обратному захвату в нервное окончание(около 50%) и вновь идет на синтез ацетилхолина.
Классификация лекарств.
1.вещества, усиливающие работу холинергического синапса
· прямого типа действия(М –Н – холиномиметики – ацетилхолин, карбохолин; М – миметики – мускарин, пилокарпин; Н – миметики – никотин, цититон, лобелин)
· непрямого типа действия:
ü антихолинэстеразные(блокируют ацетилхолинэстеразу). Делятся на вещества обратимого действия – прозерин, физостигмин, галантамин и необратимого действия – армин.
ü Вещества, усиливающие выделение ацетилхолина из нервных окончаний – аминопиридин, цисаприд(усиливает выделение ацетилхолина в кишечнике)
2.вещества, ослабляющие проведение возбуждения в холинергическом синапсе.
М – Н – холиномиметики.
Как лекарственные вещества почти не применяются, так как эффект очень краток.
Карбохолин.
Эфир карбаминовой кислоты. Действует более продолжительно(не разрушается ацетилхолинэстеразой). Используется при послеоперационной атонии гладкомышечных органов и редко в глаз для лечения глаукомы.
Рассмотрим две группы одновременно М – Н – холиномиметиков и М – холиномиметиков, так как их эффекты одинаковы(никотиновые эффекты затушевываются более сильным возбуждением мускариновых рецепторов). Выявить у лекарственного средства наличие никотинового препарата можно только, если предварительно заблокировать атропином мускариновые рецепторы.
На рисунке 10 показана схема синапса, в котором возбуждение передается с помощью ацетилхолина. Ацетилхолин синтезируется в цитоплазме холинергических нервных окончаний из ацетилкоэн-зима А и холина; путем активного транспорта проникает в везикулы и депонируется в везикулах.
При поступлении нервных импульсов происходит деполяризация мембраны нервного окончания, открываются потенциал-зависимые кальциевые каналы, ионы Са 2+ поступают в цитоплазму нервного окончания и способствуют взаимодействию белков мембраны везикул с белками пресинаптической мембраны. В результате везикулы встраиваются в пресинаптическую мембрану, открываются в сторону синаптической щели и высвобождают ацетилхолин.
Рис. 10. Холинергический синапс.
ХАТ - холинацетилтрансфераза; АцКоА - ацетилкоэнзим А; Ацх - ацетилхолин;
АХЭ - ацетилхолинэстераза.
Ацетилхолин возбуждает рецепторы постсинаптической мембраны (холинорецепторы) и расщепляется ферментом ацетилхолин-эстеразой на холин и уксусную кислоту. Холин подвергается обратному захвату нервными окончаниями (обратный нейрональный захват) и вновь участвует в синтезе ацетилхолина.
Известны вещества, действующие на разные этапы холинергической передачи.
Везамикол блокирует вход ацетилхолина в везикулы.
Ионы Mg 2+ и аминогликозиды препятствуют входу Са 2+ в нервное окончание через потенциал-зависимые кальциевые каналы (аминогликозиды могут нарушать нервно-мышечную передачу).
Ботулиновый токсин вызывает протеолиз синаптобревина (белок мембраны везикул, который взаимодействует с белками пресинаптической мембраны) и поэтому препятствует встраиванию везикул в пресинаптическую мембрану. Таким образом уменьшается выделение ацетилхолина из холинергического окончания. При ботулизме нарушается нервно-мышечная передача; в тяжелых случаях возможен паралич дыхательных мышц.
4-Аминопиридин блокирует К + -каналы пресинаптической мембраны. Это способствует деполяризации мембраны и высвобождению ацетилхолина. 4-Аминопиридин облегчает нервно-мышечную передачу.
Антихолинэстеразные вещества ингибируют ацетилхолинэстеразу и таким образом препятствуют расщеплению ацетилхолина; холи-нергическая передача активируется.
Вещества, стимулирующие холинорецепторы, называют холино-миметиками (от греч. mimesis - подражание; эти вещества в своем действии «подражают» ацетилхолину).
Вещества, которые блокируют холинорецепторы, называют хо-линоблокаторами.
Гемихолиний препятствует обратному нейрональному захвату ацетилхолина.
А. Средства, стимулирующие холинергические синапсы
Из средств, стимулирующих холинергические синапсы, в медицинской практике применяют вещества, которые стимулируют холинорецепторы - холиномиметики, а также антихолинэстеразные средства (блокируют ацетилхолинэстеразу).
Холиномиметики
Холинорецепторы разных синапсов проявляют неодинаковую чувствительность к фармакологическим веществам. Холинорецепторы клеток органов и тканей в области окончаний парасимпатических нервных волокон проявляют повышенную чувствительность к возбуждающему действию мускарина (алкалоид грибов мухоморов). Эти холинорецепторы обозначают как М-холинорецепторы (мускариночувствительные холинорецепторы).
Остальные холинорецепторы эфферентной иннервации проявляют высокую чувствительность к стимулирующему действию никотина (Nicotine; алкалоид табака), поэтому их называют N-холинорецепторами (никотиночувствительные холинорецепторы). Различают 2 типа N-холинорецепторов: N N -холинорецепторы и N м -холиноре-цепторы (рис. 11).

Рис. 11. Локализация хопинорецепторов.
Адр - адреналин; НА - норадреналин; М - М-холинорецепторы; N N - N-холинорецеп-
торы нейронального типа; N M - N-холинорецепторы скелетных мышц.
К N N -холинорецепторам относят ганглионарные N-холинорецеп-торы (N-холинорецепторы нейронов симпатических и парасимпатических ганглиев), а также N-холинорецепторы хромаффинных клеток мозгового вещества надпочечников, которые выделяют адреналин и норадреналин. Такие же рецепторы находятся в каро-тидных клубочках (расположены в местах деления общих сонных артерий); при их стимуляции рефлекторно возбуждаются дыхательный и сосудодвигательный центры продолговатого мозга.
К N M -холинорецепторам относят N-холинорецепторы скелетных мышц.
Как М-холинорецепторы, так и N-холинорецепторы имеются также в ЦНС.
В соответствии с делением холинорецепторов на М- и N-холинорецепторы холиномиметики делят на М-холиномиметики, N-холиномиметики и М, N-холиномиметики (стимулируют и М-, и N-холинорецепторы).
М-холиномиметики
Различают подтипы М-холинорецепторов - М 1 -, М 2 - и М 3 -холинорецепторы.
В ЦНС, в энтерохромаффиноподобных клетках желудка локализованы M 1 -холинорецепторы; в сердце - М 2 -холинорецепторы, в гладких мышцах внутренних органов, железах и в эндотелии сосудов - М 3 -холинорецепторы (табл. 1).
При возбуждении М,-холинорецепторов и М 3 -холинорецепто-ров через G -белки активируется фосфолипаза С; образуется ино-зитол-1,4,5-трифосфат, который способствует высвобождению Са 2+
Таблица 1. Локализация подтипов М-холинорецепторов
1 При стимуляции М 3 -холинорецепторов эндотелия кровеносных сосудов высвобождается эндотелиальный релаксирующий фактор - N0, который расширяет кровеносные сосуды.
из саркоплазматического (эндоплазматического) ретикулума. Повышается уровень внутриклеточного Са 2+ , развиваются возбудительные эффекты.
При стимуляции М 2 -холинорецепторов сердца через G.-белки угнетается аденилатциклаза, снижаются уровень цАМФ, активность протеинкиназы и уровень внутриклеточного Са 2+ . Кроме того, при возбуждении М 2 -холинорецепторов через G о -белки активируются К + -каналы, развивается гиперполяризация клеточной мембраны. Все это ведет к развитию тормозных эффектов.
М 2 -холинорецепторы имеются на окончаниях постганглионар-ных парасимпатических волокон (на пресинаптической мембране); при их возбуждении выделение ацетилхолина уменьшается.
Мускарин стимулирует все подтипы М-холинорецепторов.
Через гематоэнцефалический барьер мускарин не проникает и поэтому на ЦНС существенного влияния не оказывает.
В связи со стимуляцией М 1 -холинорецепторов энтерохромаффиноподобных клеток желудка мускарин увеличивает выделение гистамина, который стимулирует секрецию хлористоводородной кислоты париетальными клетками.
В связи со стимуляцией М 2 -холинорецепторов мускарин урежа-ет сокращения сердца (вызывает брадикардию) и затрудняет атри-овентрикулярную проводимость.
В связи со стимуляцией М 3 -холинорецепторов мускарин:
1) суживает зрачки (вызывает сокращение круговой мышцы радужки);
2) вызывает спазм аккомодации (сокращение ресничной мышцы ведет к расслаблению цинновой связки; хрусталик становится более выпуклым, глаз устанавливается на ближнюю точку видения);
3) повышает тонус гладких мышц внутренних органов (бронхи, желудочно-кишечный тракт и мочевой пузырь), за исключением сфинктеров;
4) увеличивает секрецию бронхиальных, пищеварительных и потовых желез;
5) снижает тонус кровеносных сосудов (большинство сосудов не получает парасимпатической иннервации, но содержит неиннер-вируемые М 3 -холинорецепторы; стимуляция М 3 -холинорецепторов эндотелия сосудов ведет к высвобождению N0, который расслабляет гладкие мышцы сосудов).
В медицинской практике мускарин не применяется. Фармакологическое действие мускарина может проявляться при отравлении мухоморами. Отмечаются сужение зрачков глаз, сильное слюнотечение и потоотделение, чувство удушья (усиленная секреция бронхиальных желез и повышение тонуса бронхов), брадикардия, снижение артериального давления, спастические боли в животе, рвота, диарея.
В связи с действием других алкалоидов мухоморов, обладающих М-холиноблокирующими свойствами, возможно возбуждение ЦНС: беспокойство, бред, галлюцинации, судороги.
При лечении отравлений мухоморами проводят промывание желудка, дают солевое слабительное. Для ослабления действия мускарина вводят М-холиноблокатор атропин. Если преобладают симптомы возбуждения ЦНС, атропин не используют. Для уменьшения возбуждения ЦНС применяют препараты бензодиазепинов (диазепам и др.).
Из М-холиномиметиков в практической медицине используют пилокарпин, ацеклидин и бетанехол.
Пилокарпин - алкалоид растения, произрастающего в Южной Америке. Препарат применяют в основном местно в глазной практике. Пилокарпин суживает зрачки и вызывает спазм аккомодации (увеличивает кривизну хрусталика).
Сужение зрачков (миоз) наступает в связи с тем, что пилокарпин вызывает сокращение круговой мышцы радужной оболочки (иннервируется парасимпатическими волокнами).
Пилокарпин увеличивает кривизну хрусталика. Это связано с тем, что пилокарпин вызывает сокращение ресничной мышцы, к которой прикрепляется циннова связка, растягивающая хрусталик. При сокращении ресничной мышцы циннова связка расслабляется и хрусталик принимает более выпуклую форму. В связи с увеличением кривизны хрусталика увеличивается его преломляющая способность, глаз устанавливается на ближнюю точку видения (человек хорошо видит близкие предметы и плохо - дальние). Такое явление называют спазмом аккомодации. При этом возникает мак-ропсия (видение предметов в увеличенном размере).
В офтальмологии пилокарпин в виде глазных капель, глазной мази, глазных пленок применяют при глаукоме - заболевании, которое проявляется повышением внутриглазного давления и может вести к нарушениям зрения.
При закрытоуголъной форме глаукомы пилокарпин снижает внутриглазное давление за счет сужения зрачков и улучшения доступа внутриглазной жидкости в угол передней камеры глаза (между радужкой и роговицей), в котором расположена гребешковая связка (рис. 12). Через крипты между трабекулами гребешковой связки (фонтановы пространства) происходит отток внутриглазной жидкости, которая далее поступает в венозный синус склеры - шлеммов канал (трабекуло-каналикулярный отток); повышенное внутриглазное давление снижается. Миоз, вызываемый пилокарпином, сохраняется 4-8 ч. Пилокарпин в виде глазных капель применяют 1-3 раза в день.
При открытоугольной форме глаукомы пилокарпин также может улучшать отток внутриглазной жидкости за счет того, что при сокращении цилиарной мышцы напряжение передается на трабекулы гребешковой связки; при этом происходит растяжение трабекулярной сети, фонтановы пространства увеличиваются и улучшается отток внутриглазной жидкости.
Иногда пилокарпин в малых дозах (5-10 мг) назначают внутрь для стимуляции секреции слюнных желез при ксеростомии (сухость рта), вызванной лучевой терапией опухолей головы или шеи.
Ацеклидин - синтетическое соединение, менее токсичное, чем пилокарпин. Ацеклидин вводят под кожу при послеоперационной атонии кишечника или мочевого пузыря.
Бетанехол - синтетический М-холиномиметик, который применяют при послеоперационной атонии кишечника или мочевого пузыря.

Рис. 12. Строение глаза.
N-холиномиметики
N-холиномиметиками называют вещества, возбуждающие N-xo-линорецепторы (никотиночувствительные рецепторы).
N-холинорецепторы непосредственно связаны с Nа + -каналами клеточной мембраны. При возбуждении N-холинорецепторов Na + -каналы открываются, вход Na + ведет к деполяризации клеточной мембраны и возбудительным эффектам.
N N -холинорецепторы находятся в нейронах симпатических и парасимпатических ганглиев, в хромаффинных клетках мозгового вещества надпочечников, в каротидных клубочках. Кроме того, N N -холинорецепторы обнаружены в ЦНС, в частности, в клетках Рен-шоу, которые оказывают тормозное влияние на мотонейроны спинного мозга.
N м -холинорецепторы локализованы в нервно-мышечных синапсах (в концевых пластинках скелетных мышц); при их стимуляции происходит сокращение скелетных мышц.
Никотин - алкалоид из листьев табака. Бесцветная жидкость, которая на воздухе приобретает коричневый цвет. Хорошо всасывается через слизистую оболочку полости рта, дыхательных путей, через кожу. Легко проникает через гематоэнцефалический барьер. Большая часть никотина (80-90%) метаболизируется в печени. Никотин и его метаболиты выводятся в основном почками. Период полуэлиминации (t l /2) 1-1,5 ч. Никотин выделяется молочными железами.
Никотин стимулирует в основном N N -холинорецепторы и в меньшей степени М м -холинорецепторы. В действии никотина на синапсы, имеющие на постсинаптической мембране N-холинорецепторы, по мере увеличения дозы выделяют 3 фазы: 1) возбуждение, 2) деполяризационный блок (стойкая деполяризация постсинаптической мембраны), 3) недеполяризационный блок (связан с десен-ситизацией N-холинорецепторов). При курении проявляется 1-я фаза действия никотина.
Никотин стимулирует нейроны симпатических и парасимпатических ганглиев, хромаффинные клетки надпочечников, каротидные клубочки.
В связи с тем, что никотин одновременно стимулирует на уровне ганглиев симпатическую и парасимпатическую иннервацию, некоторые эффекты никотина непостоянны. Так, обычно никотин вызывает миоз, тахикардию, но возможны и противоположные эффекты (мидриаз, брадикардия). Никотин обычно стимулирует моторику желудочно-кишечного тракта, секрецию слюнных и бронхиальных желез.
Постоянным эффектом никотина является его сосудосуживающее действие (большинство сосудов получает только симпатическую иннервацию). Никотин суживает сосуды потому что: 1)стиму-лирует симпатические ганглии, 2) увеличивает выделение адреналина и норадреналина из хромаффинных клеток надпочечников, 3) стимулирует N-холинорецепторы каротидных клубочков (рефлекторно активируется сосудодвигательный центр). В связи с сужением сосудов никотин повышает артериальное давление.
При действии никотина на ЦНС регистрируют не только возбудительные, но и тормозные эффекты. В частности, стимулируя N N -xo-линорецепторы клеток Реншоу, никотин может угнетать моносинап-тические рефлексы спинного мозга (например, коленный рефлекс). Угнетающее действие никотина, связанное с возбуждением тормозных клеток, возможно и в высших отделах ЦНС.
N-холинорецепторы в синапсах ЦНС могут быть локализованы как на постсинаптических, так и на пресинаптических мембранах. Действуя на пресинаптические N-холинорецепторы, никотин стимулирует высвобождение медиаторов ЦНС - дофамина, норадреналина, ацетилхолина, серотонина, β -эндорфина, а также секрецию некоторых гормонов (АКТГ, антидиуретический гормон).
У курильщиков никотин вызывает повышение настроения, приятное ощущение успокоения или активизации (зависит от типа высшей нервной деятельности). Повышает обучаемость, концентрацию внимания, бдительность, Снижает стрессовые реакции, проявления депрессии. Понижает аппетит и массу тела.
Эйфорию, вызываемую никотином, связывают с повышенным выделением дофамина, антидепрессивное действие и снижение аппетита - с выделением серотонина и норадреналина.
Курение. В сигарете содержится 6-11 мг никотина (смертельная доза никотина для человека около 60 мг). За время курения сигареты в организм курильщика попадает 1-3 мг никотина. Токсическое действие никотина умеряется его быстрой элиминацией. Кроме того, к никотину быстро развивается привыкание (толерантность).
Еще больший вред при курении приносят другие вещества (около 500), которые содержатся в табачном дыме и обладают раздражающими и канцерогенными свойствами. Большинство курильщиков страдают воспалительными заболеваниями органов дыхания (ларингит, трахеит, бронхит). Рак легких у курильщиков бывает значительно чаще, чем у некурящих. Курение способствует развитию атеросклероза (никотин повышает в плазме крови уровень ЛПНП и снижает уровень ЛПВП), возникновению тромбозов, ос-теопорозу (особенно у женщин старше 40 лет).
Курение во время беременности приводит к снижению массы плода, повышению послеродовой смертности детей, отставанию детей в физическом и психическом развитии.
К никотину развивается психическая зависимость; при прекращении курения курильщики испытывают тягостные ощущения: ухудшение настроения, нервозность, беспокойство, напряжение, раздражительность, агрессивность, снижение концентрации внимания, снижение познавательных способностей, депрессию, повышение аппетита и массы тела. Наиболее выражено большинство этих симптомов через 24-48 ч после прекращения курения. Затем они уменьшаются примерно в течение 2 нед. Многие курильщики, понимая вред курения, тем не менее не могут избавиться от этой вредной привычки.
Для того, чтобы уменьшить неприятные ощущения при прекращении курения, рекомендуют: 1) жевательную резинку, содержащую никотин (2 или 4 мг), 2) трансдермальную терапевтическую систему с никотином - специальный пластырь, равномерно выделяющий небольшие количества никотина в течение 24 ч (наклеивается на здоровые участки кожи), 3) мунштук, содержащий картридж с никотином и ментолом.
Указанные препараты никотина пробуют использовать в качестве лекарственных средств при болезни Альцгеймера, болезни Паркинсо-на, язвенном колите, синдроме Туретта (моторные и вокальные тики у детей) и некоторых других патологических состояниях.
Острое отравление никотином проявляется такими симптомами, как тошнота, рвота, диарея, боли в животе, головная боль, головокружение, потливость, нарушения зрения и слуха, дезориентация. В тяжелых случаях развивается коматозное состояние, нарушается дыхание, падает артериальное давление. В качестве лечебных мероприятий проводят промывание желудка, назначают внутрь активированный уголь, принимают меры борьбы с сосудистым коллапсом и нарушениями дыхания.
Цитизин (алкалоид термопсиса) и лобелии (алкалоид лобелии) сходны по строению и действию с никотином, но менее активны и токсичны.
Цитизин в составе таблеток «Табекс» и лобелии в составе таблеток «Лобесил» применяют для облегчения отвыкания от курения.
Цититон (0,15% раствор цитизина) и раствор лобелина иногда вводят внутривенно в качестве рефлекторных стимуляторов дыхания.
M.N-холиномиметики
К М,N-холиномиметикам следует отнести прежде всего ацетилхолин - медиатор, с помощью которого передается возбуждение во всех холинергических синапсах. Выпускается лекарственный препарат ацетилхолина. В клинике препарат используют редко из-за кратковременности действия (несколько минут; препарат быстро инактивируется холинэстеразой плазмы крови и ацетилхолинэсте-разой). В то же время ацетилхолин - излюбленный препарат для экспериментальной работы; кратковременность действия позволяет вводить препарат в течение исследования многократно.
Ацетилхолин возбуждает одновременно М- и N-холинорецепто-ры. Преобладает действие ацетилхолина на М-холинорецепторы. Поэтому обычно проявляются «мускариноподобные» эффекты ацетилхолина. Ацетилхолин оказывает выраженное влияние на сердечно-сосудистую систему:
1) урежает сокращения сердца (отрицательное хронотропное действие);
2) ослабляет сокращения предсердий и в меньшей степени - желудочков (отрицательное инотропное действие);
3) затрудняет проведение импульсов в атриовентрикулярном узле (отрицательное дромотропное действие);
4) расширяет кровеносные сосуды.
Большинство кровеносных сосудов не получает парасимпатической иннервации, но содержит в эндотелии и в гладких мышцах неиннервируемые М 3 -холинорецепторы. При возбуждении ацетил-холином М 3 -холинорецепторов эндотелия из эндотелиальных клеток высвобождается эндотелиальный релаксирующий фактор - N0, который вызывает расширение кровеносных сосудов (при удалении эндотелия ацетилхолин суживает сосуды - стимуляция М 3 -холинорецепторов гладких мышц сосудов). Кроме того, ацетилхолин уменьшает сосудосуживающее влияние симпатической иннервации (стимулирует М 2 -холинорецепторы на окончаниях симпатических адренергических волокон и за счет этого уменьшает выделение норадреналина).
В связи с брадикардией и расширением артерий ацетилхолин в эксперименте при внутривенном введении выражение снижает артериальное давление. Но если блокировать М-холинорецепторы атропином, большие дозы ацетилхолина вызывают не снижение, а повышение артериального давления (рис. 13). На фоне блокады М-холинорецепторов проявляется «никотиноподобное» действие ацетилхолина: возбуждение симпатических ганглиев и хромаффинных клеток надпочечников (высвобождение адреналина и норадреналина, которые суживают кровеносные сосуды).
Ацетилхолин повышает тонус бронхов, стимулирует моторику кишечника, повышает тонус детрузора мочевого пузыря, увеличивает секрецию бронхиальных, пищеварительных и потовых желез.
Путем некоторого изменения структуры ацетилхолина был синтезирован карбахолин, который не разрушается ацетилхолинэсте-разой и действует более продолжительно. Растворы карбахолина иногда используют в виде глазных капель при глаукоме.